بشر از دیرباز برای تأمین انرژی موردنیاز خود از سوختهای فسیلی استفاده میکرده است. کاهش در دسترس بودن این منابع انرژی تجدیدناپذیر به دلیل افزایش مصرف و اثرات نامطلوب ناشی از آن بر محیطزیست، محققان را بر آن داشته است تا بر روی جایگزینهایی برای آنها از میان انواع منابع انرژی تجدیدپذیر و پاک تمرکز کنند. هیدروژن یکی از گزینههای امیدوارکننده است که میتواند جایگزینی تجدیدپذیر و پاکتر برای سوختهای فسیلی مرسوم باشد [1].
یکی دیگر از مواردی که تولید هیدروژن با خلوص بالا را بسیار پر اهمیت میکند، نیاز به هیدروژن با خلوص بالا برای مصرف در فرایندهای مختلف صنعتی است. هیدروژن در چندین حوزه صنعتی به مقدار زیاد مورداستفاده قرار میگیرد. هیدروژن در پالایش نفت، سنتز آمونیاک از طریق فرآیند Haber-Bosch و فرآوری فلزاتی مانند نیکل (Ni)، تنگستن (W)، مولیبدن (Mo)، مس (Cu)، روی (Zn)، سرب (Pb) و اورانیوم (U) استفاده میشود. هیدروژن همچنین در ساخت کودهای نیتروژندار، هیدرودیسولفوریزاسیون و تصفیه هیدورژنی فرآورده های نفتی، هیدروژنه کردن پسماندهای خطرناک (PCBها، دیوکسینها و…)، سنتز اتانول، متانول و دی متیل اتر، تهیه سوختهای مایع مصنوعی به روش Fischer-Tropsch و بهعنوان سوخت کورههای صنعتی با دمای بالا و موشکهای فضایی استفاده میشود [1].
فرآیند انتقال آب-گاز[1] (WGS) یکی از قدیمیترین واکنشهای کاتالیستی ناهمگن است که در صنعت برای تولید هیدروژن با خلوص بالا و کاهش کربن مونوکسید از گاز سنتز[2] به کار میرود. واکنش WGS شامل واکنش بین CO و آب روی یک کاتالیست مناسب برای غنیسازی مخلوط گازی با H2 است. واکنش انتقال آب-گاز در حال حاضر بهطور گسترده برای تولید هیدروژن از کربن فسیلی و همچنین از ذخایر زیستتوده تجدیدپذیر استفاده میشود. بهطور سنتی، کاتالیستهای آهن-کروم (Fe-Cr) و مس-روی (Cu-Zn) به ترتیب برای تسهیل واکنش WGS در دماهای بالا و پایین استفاده میشدند. اما در طول سالها، فناوری کاتالیست واکنش WGS بهطور چشمگیری پیشرفت کرده است و برای کمک به واکنش حتی در محدوده دمای متوسط و دستیابی به تبدیل CO بالاتر، بهطور مناسبی اصلاح شده است [1, 2].
در این گزارش ابتدا نقش کاتالیستها در واکنش WGS بررسی میشود و در ادامه به نقش فناوری نانو در بهبود کارایی این کاتالیستها پرداخته میشود. در پایان نیز بازار این دسته از کاتالیستها و محصولات نانوی ایرانی در این حوزه معرفی خواهند شد.
1 نقش کاتالیستها در واکنش انتقال آب-گاز
همانطور که گفته شد، افزایش کاربردهای هیدروژن در حوزههای مختلف، منجر به توسعه مستمر آن از اواسط قرن هجدهم شده است. حدود 95 درصد از نیاز جهانی هیدروژن فعلی از طریق فرایند ریفرمینگ اولیه با بخار آب[3] تولید میشود. در این فرایند مواد کربنی طبیعی با منشأ زغالسنگ و نفت خام بهعنوان مواد اولیه به کار میروند که از جمله آنها میتوان به گاز طبیعی و برشهای سبک نفت مانند نفتا، اشاره کرد [1].
رفرمینگ متان با بخار آب در حال حاضر پرکاربردترین روش برای تولید هیدروژن است. در این فرآیند، متان و بخار آب واکنش میدهند و منجر به تولید H2 و CO میشوند. استفاده از مخلوط گازی CO و H2 در بسیاری از کاربردها امکانپذیر نیست چرا که CO منجر به مسموم شدن کاتالیست در فرایندهای پتروشیمی و الکترودهای پلاتین در پیلهای سوختی و متعاقباً منجر به غیرفعال شدن آنها میشود. واکنش انتقال آب-گاز یکی از روشهای مرسوم برای حذف CO نامطلوب در صنعت است که به کمک آن میتوان غلظت CO را در مخلوط گازی به محدوده استاندارد رساند [1, 3, 4].
گاز حاصل از ریفرمینگ که به آن گاز سنتز نیز گفته میشود، حاوی کربن مونواکسید (CO) و هیدروژن (H2) است. واکنش انتقال آب-گاز مرحله میانی است که برای کاهش درصد CO و غنیسازی هیدروژن در گاز سنتز استفاده میشود.
فرایند ریفرمینگ اولیه با بخار آب، یک مخلوط گازی تولید میکند که حاوی هیدروژن به همراه مقادیر قابلتوجهی CO است. این CO از طریق واکنش WGS مصرف میشود و در واکنش با آب به تولید CO2 و هیدروژن اضافی منجر میشود. اساساً مخلوطی از CO و بخار آب از طریق واکنش WGS به CO2 و H2 تبدیل میشود:
CO + H2O ↔ CO2 + H2 ΔH298°C = – 41.09 kJ.mol-1
این واکنش نسبتاً گرماده است به همین دلیل وقوع آن به لحاظ ترمودینامیکی در دمای پایین و به لحاظ سینتیکی در دمای بالا محتملتر است اما تغییر فشار، تأثیری بر آن ندارد. فرایند WGS فرایندی مهم برای تولید هیدروژن عاری از CO و یا تنظیم نسبت H2/CO است [1].
برای دستیابی به هیدروژن با خلوص بالا و در مقیاسهای صنعتی از گاز سنتز، نیاز به انتخاب کاتالیست مناسب برای تسهیل در انجام واکنش است. کاتالیستهای WGS در دو دسته کلی قرار میگیرند: کاتالیستهای انتقال دما بالا (HTS[4]) و کاتالیستهای انتقال دما پایین ([5]LTS). در ابتدا کاتالیستهای آهن اکسید-کروم اکسید برای واکنشهای WGS معرفی شدند که در خط تولید آمونیاک مورداستفاده قرار میگرفتند. این کاتالیستها این توانایی را داشتند تا بتوانند غلظت CO را به 2 تا 4% مولی در گاز خروجی برسانند. این کاتالیستها تنها در دمایی بین 310 تا 450 درجه سانتیگراد فعال بودند و به همین دلیل به کاتالیستهای انتقال دما بالا معروف شدند. فعالیت کاتالیستی این دسته از کاتالیستها با کاهش دما به شدت کاهش مییابد. همچنین به دلیل درصد به نسبت بالای CO در گاز خروجی برای رسیدن به غلظت 1% مولی برای CO در هیدروژن خروجی، نیاز است تا فرایند با استفاده از چندین راکتور و بستر کاتالیستی به وقوع بپیوندد و میان هر راکتور نیز سامانه خنکسازی وجود داشته باشد [1, 3].
بعد از این دسته از کاتالیستها، نوع جدیدی از کاتالیستها معرفی شدند که بر پایه مس بودند و در دمای پایینتری در حدود 200 درجه سانتیگراد عمل میکردند. غلظت CO در گاز خروجی در حضور این کاتالیستها بین 0.1 تا 0.3% مولی بود و به کاتالیستهای انتقال دما پایین شناخته شدند. کاتالیستها پایه مس نسبت به ترکیبات گوگردی موجود در هیدروکربنها حساس هستند و غیرفعال میشوند در حالی که کاتالیستهای بر پایه آهن چندان به گوگرد حساس نیستند [1].
واکنش WGS بهصورت تجاری و در صنعت با استفاده از دو راکتور آدیاباتیک انجام میشود که در بخش اول انتقال دما بالا به وقوع میپیوندد (راکتور HTS) و در ادامه در بخش دوم، انتقال دما پایین رخ میدهد (راکتور LTS) و میان این دو بخش، سامانه سرمایش برای کاهش دما تعبیه میشود تا دمای ورودی مرحله دوم برای انتقال دما پایین مناسب باشد (شکل 1). دمای بالا در راکتور اول موجب میشود به لحاظ سینتیکی بهینهتر باشد و سرعت بالای مصرف شدن CO را در پی دارد و موجب میشود که درصد بالای CO با سرعت بالایی کاهش یابد. در راکتور دوم بهینهسازی ترمودینامیکی مدنظر است و از این رو دما پایینتر است و انتخابپذیری بالاتری برای مصرف CO که طی مرحله قبل، غلظت آن به شدت کاهش یافته است، دارد. به همین دلیل میتواند غلظت آن را به 0.1 تا 0.3 درصد برساند. همچنین برای محافظت از کاتالیست مس در برابر گوگرد یک بستر محافظ پیش از راکتور LTS قرار داده میشود تا ترکیبات حاوی گوگرد را به حداقل برساند [1, 3].
 شکل 1- طرح کلی فرایند تولید و CO زدایی از H2 برای تولید آمونیاک. گام اول در فرآیند تولید آمونیاک، تولید هیدروژن از گاز طبیعی است که شامل چندین فرآیند متمایز است. در ابتدا، گاز سنتز از گاز طبیعی با استفاده از فرآیند ریفرمینگ تولید میشود. سپس، مونوکسیدکربن با استفاده از راکتورهای شیفت در واکنش با بخار آب به هیدروژن و کربن دی اکسید تبدیل میشود. انتقال آب گاز در دو راکتور سری که اولی دما بالا و دومی دما پایین است، انجام میشود. قبل از تولید گاز سنتز، گاز طبیعی باید عاری از آلودگیهایی باشد که اثرات نامطلوبی بر کاتالیزورهای پایین دست دارد و بایستی حذف شود. گاز طبیعی معمولاً حاوی غلظتهای مختلفی از ترکیبات گوگردی به شکل سولفید هیدروژن و یا اجزای حاوی گوگرد آلی است [5].
شکل 1- طرح کلی فرایند تولید و CO زدایی از H2 برای تولید آمونیاک. گام اول در فرآیند تولید آمونیاک، تولید هیدروژن از گاز طبیعی است که شامل چندین فرآیند متمایز است. در ابتدا، گاز سنتز از گاز طبیعی با استفاده از فرآیند ریفرمینگ تولید میشود. سپس، مونوکسیدکربن با استفاده از راکتورهای شیفت در واکنش با بخار آب به هیدروژن و کربن دی اکسید تبدیل میشود. انتقال آب گاز در دو راکتور سری که اولی دما بالا و دومی دما پایین است، انجام میشود. قبل از تولید گاز سنتز، گاز طبیعی باید عاری از آلودگیهایی باشد که اثرات نامطلوبی بر کاتالیزورهای پایین دست دارد و بایستی حذف شود. گاز طبیعی معمولاً حاوی غلظتهای مختلفی از ترکیبات گوگردی به شکل سولفید هیدروژن و یا اجزای حاوی گوگرد آلی است [5].
———————————————————
[1] Water-Gas Shift (WGS)
[2] Syn-Gas
[3] Steam Reforming
[4] High Temperature Shift Catalysts
[5] Low Temperature Shift Catalysts
ترکیب کاتالیست HTS بهطور مرسوم، 74.2٪ Fe2O3، 10.0٪ Cr2O3، 0.2٪ MgO و باقیمانده آن، ترکیبات فرار هستند. ترکیب شیمیایی کاتالیست LTS نیز مخلوطی از CuO، ZnO و Al2O3/Cr2O3 است که دو مثال از ترکیبات مرسوم کاتالیستهای LTS به شرح زیر است [4]:
- 68-73٪ ZnO، 15-20٪ CuO، 9-14٪ Cr2O3، 2-5٪ Mn و مابقی اکسیدهای Al و Mg
- 32-33٪ CuO، 34-53٪ ZnO و 15-33% Al2O3
کاتالیستهای LTS از طریق تزریق همزمان محلول اسیدی (خوراک) حاوی یونهای فلزی مس، روی و آلومینیوم از یکسو و محلول قلیایی تنظیمکننده pH (بهعنوان مثال کربنات سدیم) از سوی دیگر حاصل میشود. مقدار pH باید در تمام طول تزریق (ترسیب) در محدوده مطلوب، ثابت بماند [6].
1 کاتالیستهای WGS دما پایین بر پایه مس
اولین کاتالیست WGS دما پایین بر پایه مس در سال 1963 معرفی شد که از CuO و ZnO با نسبت 1 به 2، تشکیل شده بود. کمی بعد مشخص شد که افزودن آلومینا به ساختار این کاتالیستها میتواند پایداری گرمایی را افزایش دهد و مقاومت در برابر مسموم شدن کاتالیست را بهبود بخشد. از این رو کاتالیستهای ترکیبی از اکسیدهای CuO، ZnO و Al2O3 بهصورت تجاری و بهطور گستره مورداستفاده قرار گرفتند. فلز مس موجود در این کاتالیستها فعالیت کاتالیستی و انتخابپذیری بالایی را در دمای پایین از خود نشان میداد بنابراین کاتالیست مناسبی برای واکنش WGS در دمای پایین و در غلظت کم CO بود. این کاتالیستها در بازه 150 تا 280 درجه سانتیگراد فعال هستند و مقدار بهینه آن بین 200 تا 280 درجه سانتیگراد است. کاهش CuO و دیگر ترکیبات شیمیایی حاوی مس، یک عامل مهم برای افزایش فعالیت کاتالیستی است. از طرفی فعالیت کاتالیستی این دسته از کاتالیستها متناسب با سطح در دسترس از مس فلزی است و چندان به نسبت Al/Zn وابسته نیست. فعالیت کاتالیستی کاتالیستهای سهتایی معرفی شده وابستگی زیادی به تشکیل ساختار اسپینل از اکسیدهای Cu-Al-Zn دارد چرا که منجر به تشکیل ذرات بسیار ریز مس بر روی سطح پایه کاتالیست میشود و سطح فعال را افزایش میدهد. بر اساس مطالب گفته شده، برای بهبود کارایی این دسته از کاتالیستها نخست باید شرایطی فراهم شود که ذرات فلزی مس در کوچکترین اندازه بر روی سطح پراکنده شوند و دیگر آنکه این ذرات در طول فرایند کاتالیستی، تجمع نکنند و به هم نپیوندند و ذرات بزرگتری را تشکیل ندهند. این نقش را تا حد زیادی حضور Al2O3 ایفا میکند و در واقع نقش یکی پروموتر ساختاری[1] را دارد [3].
2 فناوری نانو برای بهبود کاتالیستهای WGS
کاتالیستهای بر پایه مس در کنار مزایایی که دارند از مشکل غیرفعال شدن[2] رنج میبرند. سه دلیل عمده برای این پدیده گزارش شده است:
- تف جوشی گرمایی که منجر به کاهش سطح ویژه کاتالیستی میشود.
- مسموم شدن توسط گوگرد که مسدود شدن نواحی فعال کاتالیستی و کاهش سرعت جابهجایی واکنشدهندههایی که بر روی سطح جذب شدهاند را در پی دارد.
- مسموم شدن توسط کلر که تف جوشی کاتالیست و در نتیجه درشت شدن ذرات ماده فعال را سرعت میبخشد.
از این رو در کنار استفاده از کاتالیستهای مرسوم و سنتی مس-روی همواره تلاشهای فراوانی برای معرفی کاتالیستهایی با بازده بالاتر، پایداری و انتخابپذیری بیشتر موردتوجه بوده است. این تلاشها در دو دسته کلی قرار میگیرند:
- معرفی کاتالیستهایی با ترکیب شیمیایی جدید از طریق بررسی اثر توأمان ماده فعال و پایه کاتالیست بر روی ویژگیهای مطلوب کاتالیست
- استفاده از نانوساختارها
از این رو از طرفی کاتالیستهای نوینی بر پایه سریا (CeO2)، کاتالیستهای جدید بر پایه کربن و کاتالیستهای بر پایه فلزات نجیب، معرفی شدهاند و از طرف دیگر، کاتالیستهای مرسوم و یا کاتالیستهای جدید در ابعاد نانومتری تولید و موردبررسی قرار گرفتهاند. در نتیجه میتوان گفت که فناوری نانو مسیرهای فراوانی را برای بهبود خواص این دسته از کاتالیستها گشوده است. در زمینه بهبود خواص کاتالیست WGS، هم بر روی ماده فعال کاتالیستی و هم بر روی پایه کاتالیست، تمرکز شده است. در مورد تأثیر فناوری نانو بر روی کاتالیستها میتوان گفت که با کوچک شدن اندازه ذرات در ابعاد نانومتری، سطح ویژه فعال بیشتری جهت فرایندهای کاتالیستی در دسترس قرار میگیرد [1, 3].
در کنار کاتالیستهای بر پایه آهن و مس کاتالیستهای بر پایه نیکل، کبالت، مولیبدن، طلا، پلاتین، رودیم و روتنیم از دیگر مواد فعال کاتالیستی برای واکنش WGS محسوب میشوند. همچنین مرسومترین پایه کاتالیستها در این حوزه، Al2O3، ZnO و SiO2 هستند. پایه کاتالیستهای TiO2 و CeO2 نیز جزء پایه کاتالیستهای نوین هستند که به دلیل توانایی در ذخیرهسازی اکسیژن، خواص عالی بهعنوان پروموتر ایفا کردهاند. کبالت و مولیبدن به لحاظ مقاومت در برابر مسموم شدن با گوگرد خواص مناسبی را از خود نشان دادهاند. فلزات نجیب نیز فعالیت کاتالیستی بالایی برای واکنش WGS دارند اما فعالیت کاتالیستی آنها به شدت به پایه کاتالیست وابسته است [1, 4].
یکی از موادی که به شدت بهعنوان پایه کاتالیست برای جایگزینی با کاتالیستهای مرسوم WGS مدنظر قرار دارد، سریا (CeO2) است. گرچه سریا و مواد بر پایه سریا فعالیت کاتالیستی مناسبی برای واکنش WGS از خود نشان ندادهاند اما به دلیل وجود جای خالی اکسیژن و ذخیرهسازی اکسیژن در داخل ساختار خود، مشاهده شده است که در هنگامی که بهعنوان پایه کاتالیست مورداستفاده قرار میگیرد، به خوبی بهعنوان یک پروموتر میتواند میزان فعالیت کاتالیستی را افزایش دهد. همانطور که پیشتر گفته شد مس یکی از کاتالیستهای مرسوم LTS است. پژوهشها نشان داده است که مس، چه بهصورت ذرات بر روی سطح سریا بهعنوان پایه کاتالیست و چه بهصورت مس عنصری حل شده در ساختار سریا، فعالیت کاتالیستی مناسبی از خود نشان داده است [1].
همچنین مشاهده شده است که اگر چه طلا در ابعاد بزرگ در واکنش WGS فعالیت کاتالیستی اندکی از خود نشان میدهد اما نانوذرات طلا بر روی پایه کاتالیست سریا، نه تنها فعالیت کاتالیستی دارند بلکه بازده واکنش بالایی را از خود نشان میدهند. بازده واکنش کاتالیستی در ابعاد نانومتری، بیش از مقدار طلا متأثر از اندازه ذرات طلاست. اندازه نانوذرات طلا در این حالت با توجه به روش تولید، 2 تا 6 نانومتر است و بیشترین فعالیت کاتالیستی را نانوذرات طلای 2 نانومتری از خود نشان داده است. با آلاییدن[3] کاتالیست طلا-سریا با فلزات La و Gd نیز شاهد افزایش فعالیت کاتالیستی خواهیم بود [1, 4].
استفاده از سریا بهعنوان پایه کاتالیست و نشاندن نانوذرات فلزات واسطه (Fe، Ni، Cr و…) یا فلزات نجیب (Pt، Pd و…) بر روی آن از دیگر تلاشهایی است که برای معرفی یک کاتالیست بهینه برای فرایند WGS در حال انجام است. در این دسته از کاتالیستها سریا نیز میتواند نانوساختار باشد که استفاده از نانوساختارهای تکبعدی مانند نانوالیاف سریا بهعنوان پایه کاتالیست به شدت موردتوجه قرار دارد [1].
از دیگر مسیرهای مبتنی بر فناوری نانو برای دستیابی به کاتالیستهای WGS بهینه میتوان به کاتالیستهای با پایه کاتالیست کربنی اشاره کرد. کربن فعال یکی از پایه کاتالیستهای مناسبی است که برای این دسته از کاتالیستها به نحو مطلوبی عمل میکند. فعالیت کاتالیستی کربن فعال همراه با نانوذرات آهن اکسید، مس و فلزات نجیب، بر روی واکنش WGS نتایج مناسبی در پی داشته است. همچنین نانولوله کربنی بهعنوان پایه کاتالیست با انواع مواد فعال فلزی و اکسید فلزی، موردبررسی قرار گرفته است [1, 3].
3 محصولات داخلی
با توجه به اهمیت کاتالیست انتقال آب-گاز دما پایین برای کشور و محدودیتهایی که در تأمین آن وجود دارد، این کاتالیست توسط شرکت دانشبنیان گسترش فناوری خوارزمی بومیسازی شده است. شرکت دانشبنیان گسترش فناوری خوارزمی با بیش از ۱۵ سال سابقه پژوهش و فناوری، فعالیت خود را در جهت توسعه دانش فنی تولید کاتالیستهای صنعتی در ایران، رسماً از سال ۱۳۸۹ آغاز کرد و در حال حاضر موفق به تولید طیف گستردهای از کاتالیستهای مورداستفاده در صنعت فولاد، پالایش و پتروشیمی شده است [6].
—————————
[1] Structural Promoter
[2] Deactivation
[3] Doping
علاوه بر نانوکاتالیست انتقال آب-گاز دما پایین، انواع کاتالیستهای ریفرمینگ احیای مستقیم، انواع کاتالیست ریفرمینگ دارای کاربرد در پالایشگاهها و صنایع پتروشیمی، کاتالیست اتوترمال، کاتالیست انتقال آب ـ گاز دما بالا، کاتالیستهای پیش ریفرمینگ، کاتالیستهای متاناسیون، کاتالیستهای سنتز متانول و کاتالیستهای هیدرودیسولفوریزاسیون از دیگر محصولات این شرکت است [2].
فلز فعال کاتالیستی در کاتالیست LTS تولید شده توسط گسترش فناوری خوارزمی، مس است که پس از احیای کاتالیست درون راکتور و تبدیل اکسید مس به مس، خاصیت کاتالیستی پیدا میکند. برای بیشینه کردن کارایی این کاتالیستها لازم است که آنها بیشترین سطح فعالیت کاتالیستی را داشته باشند. با ورود فناوری نانو به این صنعت و تولید نانوکاتالیستهای با سطح فعال قابل توجه، تحولی عظیم در کارایی آنها بهوجود آمده است. دستیابی به ریزساختار نانو حاوی ذرات با ابعاد کمتر از 20 نانومتر در این محصول سطح فعال بیشتر برای محصول و به دنبال آن اکتیویته بیشتری را به همراه داشته است. بهمنظور بررسی خاصت کاتالیستی این محصول، آزمون در سیستم کاتالیستی (Catatest) روی نمونه تولید شده و یک نمونه صنعتی (شرکت Sud-Chemie) انجام و گازهای خروجی با استفاده از دستگاه کروماتوگرافی اندازهگیری شد. مقایسه نتایج حاصل از آزمون کاتالیستی نمونه تولید شده و نمونه صنعتی، بیانگر انطباق بسیار مناسب این دو محصول است (شکل 2) [2].
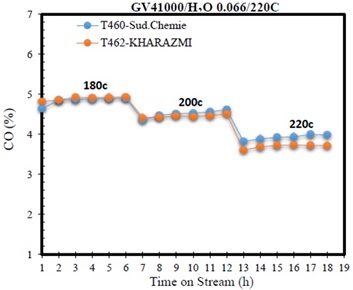 شکل 2- مقایسه خاصیت کاتالیستی کاتالیست LTS شرکت گسترش فناوری خوارزمی و شرکت Sud Chemie [2].
شکل 2- مقایسه خاصیت کاتالیستی کاتالیست LTS شرکت گسترش فناوری خوارزمی و شرکت Sud Chemie [2].
6 بازار داخلی و جهانی کاتالیستها
اندازه بازار جهانی کاتالیستها در سال 2022، 24.2 میلیارد دلار بوده است که با رشد سالانه 4.2 درصد تا سال 2032 به 36.4 میلیارد دلار افزایش خواهد یافت. به لحاظ جنس کاتالیستها مشاهده میشود که کاتالیستهای فلزی پس از ترکیبات شیمیایی، بیشترین مقدار را به خود اختصاص دادهاند [7].
از منظر کاربرد، کاتالیستها در چهار کاربرد عمده تقسیمبندی میشوند: سنتز شیمیایی، پالایش نفت، کاربردهای محیطزیستی و پلیمر و پتروشیمی که از میان آنها در سال 2022، سنتز شیمیایی با 26.3 درصد، بیشترین سهم بازار را در اختیار داشته است (شکل 4) [7].
بازار کاتالیستها بازار روبه رشدی است. بهطور خاص در مورد کاتالیستهای انتقال آب-گاز نیز بازار روبه رشدی پیشبینی میشود. توسعه صنایع مصرفکننده هیدروژن همچون نفت، گاز و پتروشیمی، صنایع شیمیایی و صنایع فلزی و همچنین توجه فراوان به هیدروژن بهعنوان سوخت پاک، دو پیشران اصلی در جهت رشد و توسعه این کاتالیستها محسوب میشوند.
در بازار داخلی نیز به دلیل توسعه صنعت پتروشیمی، بازار روبه رشدی برای کاتالیستهای LTS پیشبینی میشود. بهعنوان مثال با توجه به تعداد واحدهای فعلی و برنامه آتی توسعه تولید آمونیاک در ایران (مجموعاً ۱۴ واحد)، تولید کاتالیست واحد LTS حائز اهمیت فراوان است. از این رو لازم است تا نیازهای اساسی و استراتژیک این صنعت (همچون کاتالیست) در داخل کشور تأمین و تولید شود. میزان مصرف سالانه کاتالیست انتقال دما پایین یا LTS در کشور ۳۵۰ تن در سال است و با احتساب قیمت خرید این کاتالیست از منابع خارجی که در حدود ۲۰ یورو به ازای هر کیلوگرم است، بومیسازی تولید این محصول میتواند علاوه بر افزودن دانش فنی تولید یک محصول استراتژیک صنعتی به توانمندیهای کشور، سالیانه از ارزبری معادل ۷ میلیون یورو جلوگیری کند [6].
مراجع
[1] D. B. Pal, R. Chand, S. Upadhyay, and P. Mishra, “Performance of water gas shift reaction catalysts: A review,” Renewable and Sustainable Energy Reviews, vol. 93, pp. 549-565, 2018.
[2] Nanoproduct, “https://nanoproduct.ir/product/2813; کاتالیست انتقال آب-گاز دما پایین,” 1398.
[3] E. Baraj, K. Ciahotný, and T. Hlinčík, “The water gas shift reaction: Catalysts and reaction mechanism,” Fuel, vol. 288, p. 119817, 2021.
[4] P. Ebrahimi, A. Kumar, and M. Khraisheh, “A review of recent advances in water-gas shift catalysis for hydrogen production,” Emergent Materials, vol. 3, pp. 881-917, 2020.
[5] Khwarizmico, “https://khwarizmico.com/products/petrochemical-catalysts/ammonia-units; واحدهای آمونیاک ” 1402.
[6] Nanoproduct, “https://nanoproduct.ir/news/66302; فناوری نانو کاتالیستها را کارآمدتر میکند,” 1398.
[7] Market.Us, “https://market.us/report/catalyst-market/,” 2023.
————————————————————-
ترویج صنعتی فناوری های نانو و میکرو
====================================================================================
[جهت دسترسی به گزارش نهایی محصولات و شرکتهای دارای گواهی نانومقیاس ستاد توسعه فناوریهای نانو و میکرو به «کتب مرجع محصولات و تجهیزات نانو و صنعت» به نشانی (INDnano.ir/category/book) مراجعه کنید]
[همچنین برای دانلود فایل PDF کلیه گزارشات بهمراه جزئیات، به بخش گزارش های صنعتی پایگاه اینترنتی رسانه تخصصی نانو و صنعت (www.INDnano.ir/category/report) مراجعه نمایید]
====================================================================================













