نانوپزشکی، کاربرد فناوری نانو در حوزههای مختلف علوم پزشکی و سلامت است. یکی از این حوزهها داروسازی و دارورسانی میباشد. پیشبینی میشود که نانوزیست فناوری بتواند بیشتر داروهایی را که از اجزائی با ابعاد نانومتری بوجود میآیند متحول نماید. بکارگیری روشهای نوین در هدفمند ساختن داروها و اثرگذاری آنها بر بخشهای مشخص اهمیت فراوان دارد. بکارگیری روشهای نانومتری از چند جهت در طراحی و ساخت داروها حائز اهمیت است که از جمله میتوان به اندازهگیریها، آزمایشها، محاسبات و تواناییها اشاره کرد. همچنین، چون بسیاری از این دست داروها برخلاف روشهای موجود، دارای فعالیتهای قابل فهمتری هستند، امکان کاهش زمان طراحی تا تولید انبوه در آنها بسیار بالا خواهد بود. برای اینکه یک دارو از جهت درمانی موثر بماند لازم است تا رسیدن به محل اثر محافظت شود و ویژگیهای زیستی و شیمیایی آن حفظ گردد.
بعضی دیگر از داروها بسیار سمی بوده و سبب بروز عوارض جانبی بسیار نامطلوب شده و اگر در طی انتقال به درون بدن از هم پاشیده شوند، اثرات درمانی آنها کاهش خواهد یافت. مشکلات موجود در زمینه دارورسانی بسیار زیاد و متفاوت خواهد بود. سامانههای دارورسانی از جهت بکارگیری مواد و فرآیند تولید محدودیت زیادی دارند. مواد این سامانهها باید سازگاری زیستی با بدن داشته باشند و به آسانی به دارو متصل شوند و از بدن قابل حذف باشند. فرآیند تولید نیز به شدت کنترل شود تا محصول متلاشی نگردد و از لحاظ قیمت نیز مناسب باشند. نانوفناوری در زمینههای دارورسانی میتواند راهحلهای جدیدی را ارائه کند.
2- لیپوزومها
لیپوزوم عبارتست از یک وزیکول[1] میکروسکوپی شامل دو لایه فسفولیپیدی که یک فضای آبی را احاطه نموده است. ضخامت این لیپید دو لایه به طور معمول بین 3 تا 6 نانومتر است و لیپوزومهای تشکیل شده از آنها میتوانند قطری بین 50 نانومتر تا 50 میکرومتر داشته باشند. لیپوزومها به دلیل خاصیت آمفیپاتیک[2] (دوگانه دوست) عناصر سازنده آن، امکان دارورسانی داروهای آبدوست و یا چربی دوست را فراهم مینمایند. این ساختارهای ریز و کیسه مانند، شبیه بستهها یا کپسولهایی هستند که میتوان با به دام انداختن دارو درونشان (انکپسولاسیون)[3]، از آنها برای حمل دارو به نقاط مختلف بدن استفاده کرد.
2-1- تاریخچه
لیپوزوم، بیش از 45 سال زمینه تحقیقات گستردهای برای محققان علاقمند به این حوزه بوده است. امکان حضور ساختارهای وزیکول مانند، در سیستمهای آبی حاوی مولکولهای دوگانهدوست اولین بار بوسیله Bernard هنگام مطالعات میکروسکوپی اشکال میلین[4] تشکیل شده با آمونیوم اولئات[5] در آب فرض گردید (Bernard et al., 1947). در سال 1992 Bangham با استفاده از میکروسکوپ الکترونی در کمبریج، پراکندگی فسفولیپیدها را در آب به وسیله رنگآمیزی منفی با استفاده از سدیم فسفو تنگستات و آمونیوم مولیبدات بررسی کرد و شواهد آزمایشهای نهایی نشان داد که فسفولیپید به طریق خودآرایی[6] تشکیل ساختار کیف مانندی میدهد که لیپوزوم نامیده شد (Bangham, 1992).
3- ویژگیهای ساختاری لیپوزومها
ساختار لیپوزومها، بازگوکننده بخشی از خواص منحصر به فرد آنها در دارورسانی است. از اینرو شناخت ساختار لیپوزومها به درک بهتری از مکانیسم عمل لیپوزومها و همچنین نقاط ضعف و قوت این سامانههای دارورسانی نوین کمک میکند. بیشتر لیپوزومهای سنتز شده از مولکولهای دوگانهدوست لیپیدی به نام فسفولیپید تشکیل شدهاند. ساختار فسفولیپیدها متشکل از یک گروه الکلی به عنوان اسکلت فسفولیپیدی (که گلیسرول یا اسفنگوزین هستند)، دو مولکول اسید چرب، فسفات، و گروههای متصل به فسفات میباشد (شکل-1). انتهای یک سر فسفولیپیدها گروه فسفات (آبدوست) و انتهای سر دیگرشان دارای اسید چرب است (بعلت وجود ساختار هیدروکربنی آبگریز است).
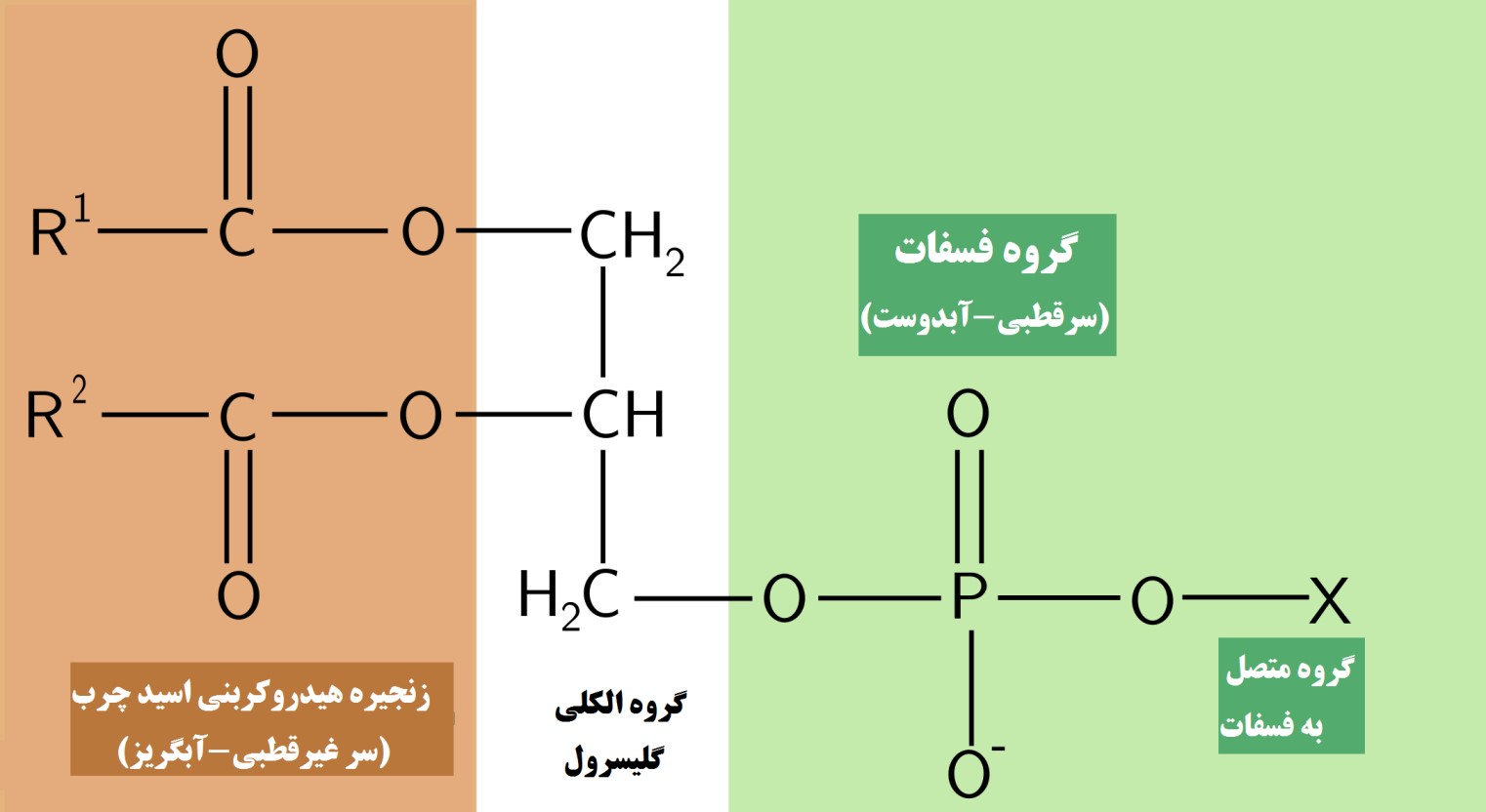 شکل-1. ساختار فسفولیپیدها
شکل-1. ساختار فسفولیپیدها
لیپوزومها از اجتماع این فسفولیپیدها در محیط آبی به دور هم به وجود می آیند. شکل2 نمایی از لیپوزوم را نشان میدهد.
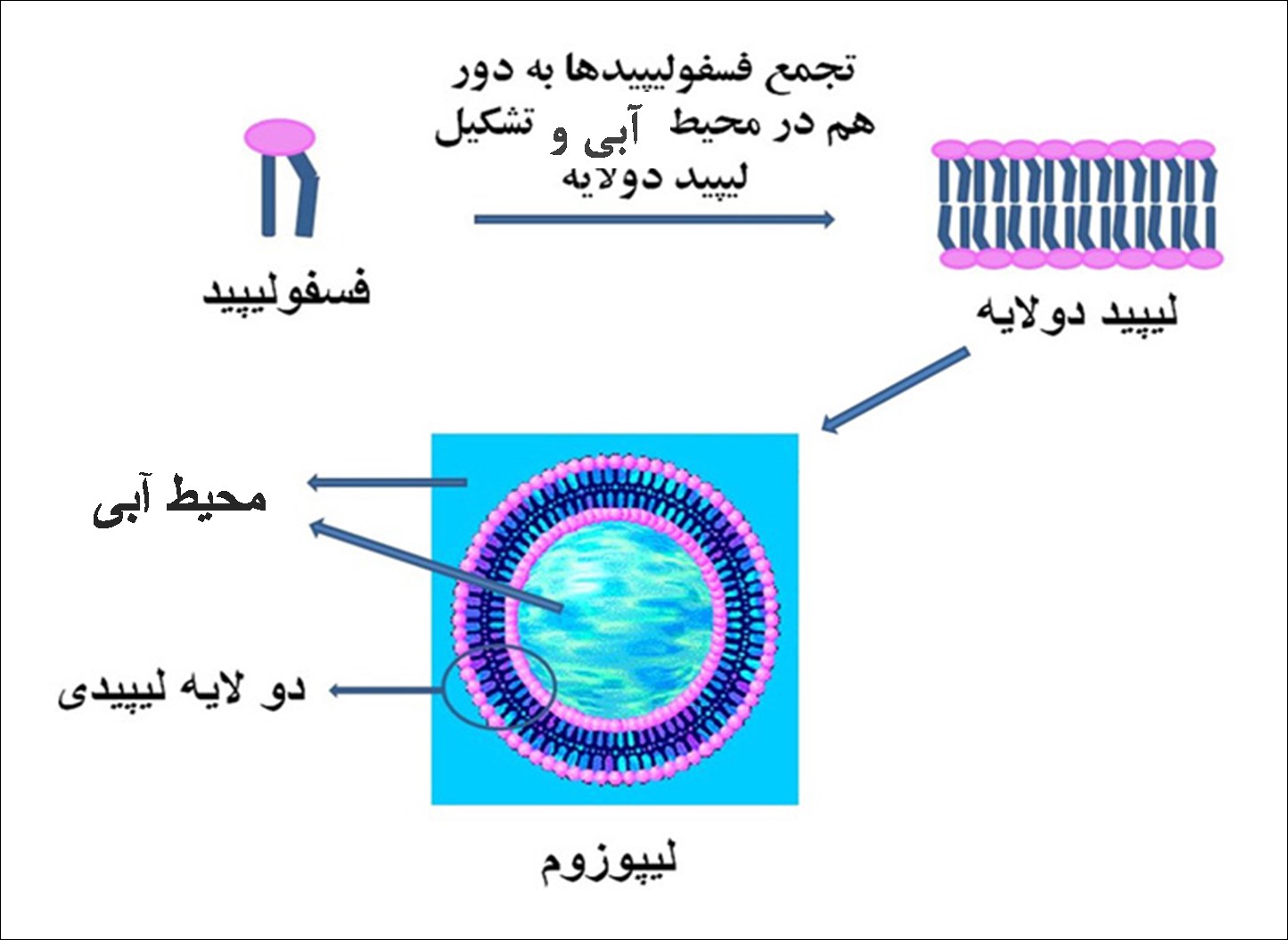 شکل-2. نمایی از ساختار فضایی لیپوزوم
شکل-2. نمایی از ساختار فضایی لیپوزوم
3-1- انواع روشهای سنتز لیپوزوم
در سامانههای دارورسانی لیپوزومی، در سنتز محصولات دو هدف مهم مورد توجه است، یکی سنتز لیپوزومهای مورد نظر و دومی بازده به دام انداختن دارو در درون آنها یا به اصطلاح بارگیری دارو در درون لیپوزومها. روشهای بسیار متنوعی برای تهیه لیپوزومها ابداع شده و تکامل پیدا کرده است، اما تعداد محدودی از آنها قادر به به دام انداختن[7] مقادیر زیاد داروهای محلول در آب هستند.
روش کلی سنتز لیپوزومها در 3 یا 4 مرحله طبق جدول زیر خلاصه میگردد:
جدول-1. مراحل کلی سنتز لیپوزومها
| مراحل سنتز | توضیح |
| 1- خشک کردن چربی از حلال آلی | ابتدا باید مولکولهای چربی یا فسفولیپیدها را در یک محلول آلی حل کرد، سپس این محلول آلی را با یک محلول آبی جایگزین کرد. در نتیجه، حلال آلی را از محیط محلول، بوسیله تبخیر یا فرایندهای دیگر خارج میکنند. |
| 2- پراکندگی چربی در محیط آبی | محلول آبی را جایگزین محلول آلی میکنند تا مولکولهای چربی در درون این محیط پراکنده شده و تشکیل لیپوزومهای متنوعی دهند. |
| 3- تخلیص لیپوزومهای حاصل | لیپوزومهایی با اندازه و نوع مورد نظر را میتوان از بین مواد سنتزی جدا کرد. |
| 4- آنالیز محصولات نهایی | خواص و ویژگیهای لیپوزومهای خالص شده را میتوان توسط ابزار و تکنیکهای مختلف شناسایی کرد. |
دو روش کلی در تهیه لیپوزومها بر پایه بارگیری دارو وجود دارد:
- روشهای بارگیری غیرفعال: در این شیوه به دام انداختن داروها، قبل از ساخت یا در طی ساخت لیپوزوم است. این روش به سه دسته تقسیم میشود که هر کدام شامل روشهای مختلفی هستند. جدول-2 تقسیمبندی این روش را نشان میدهد.
جدول-2. روشهای بارگیری غیر فعال
| Lipid film hydration by hand shaking, non-hand shaking or Freeze drying | آبکافت فیلم چربی بوسیله تکان دادن دستی، غیر دستی یا خشک کردن انجمادی (Freeze drying) |
1. روشهای انتشار مکانیکی |
روشهای بارگیری غیر فعال |
| Micro-emulsification | میکروامولسیفیکاسیونی | ||
| Sonication | سونیکاسیون | ||
| French pressure cell | سلول فشار فرانسوی | ||
| Membrane extrusion | انفصال غشائی | ||
| Dried reconstituted vesicles | وزیکولهای آماده شده خشک | ||
| Freeze-thawed liposomes | لیپوزومهای گداخته شده منجمد | ||
| Ethanol injection | تزریق اتانول | 2. روشهای انتشار حلال | |
| Ether injection | تزریق اتر | ||
| Double emulsion | وزیکولهای امولسیون دوتایی | ||
| Reverse phase evaporationvesicles | وزیکولهای فاز بخار معکوس | ||
| Stable pluri lamellar vesicles | وزیکولهای چند لایه پایدار | ||
| Detergent removal from mixemicells by: Dialysis, Column chromatography, Dilution | حذف دترجنت از مخلوط میسلها به وسیله دیالیز، ستون کروماتوگرافی، رقیق سازی | 3. روشهای حذفی دترجنت |
در این روشها، داروهای آبدوست در محیط آبی درون لیپوزومها انکپسوله میشوند و داروهای آبگریز (چربی دوست) در بین دو لایه فسفولیپیدی محصور میگردند. مواد محلول در آب، به محلول آبیای اضافه میشوند که بین توده و تجمع سرهای آبگریز به دام افتاده است و مواد محلول در چربی در بین دو لایه فسفولیپیدی جا داده می شوند. شکل-3 انکپسولاسیون دارو را درون لیپوزومها نشان میدهد.
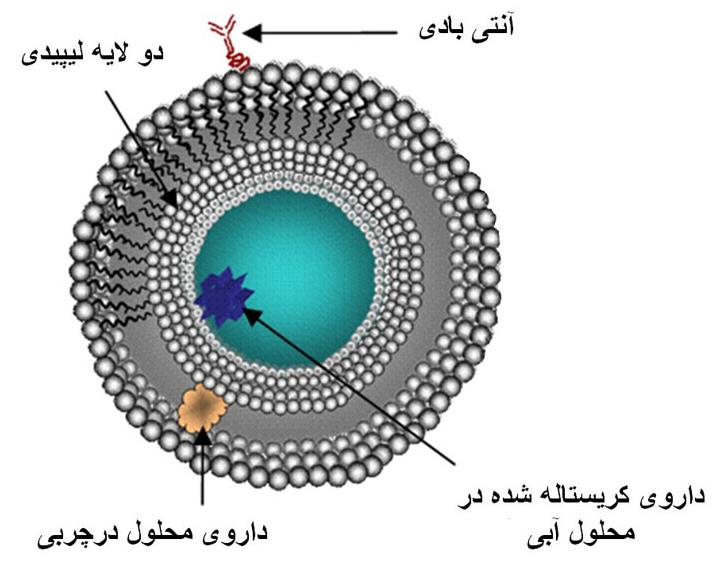 شکل-3. انکپسولاسیون دارو درون لیپوزومها
شکل-3. انکپسولاسیون دارو درون لیپوزومها
- روشهای بارگیری فعال: به نوع مشخصی از ترکیبات با گروههای یونیزه شونده و یا ترکیباتی که هم در آب و هم در چربی محلولاند و میتوانند به داخل لیپوزومها بعد از مرحله تشکیلشان نفوذ کنند، مربوط میشود.
3-2- تقسیم بندی لیپوزومها بر اساس روشهای مختلف
- تقسیمبندی لیپوزومها بر اساس پارامترهای ساختاری
اساس این تقسیمبندی، اندازه لیپوزومها و همچنین تعداد لایههای تشکیلدهنده لیپوزومها است. اندازه لیپوزومها فاکتور بسیار مهمی در کاربردهای بالینی و نوع تجویز دارو (پوستی، درون رگی و غیره) است.
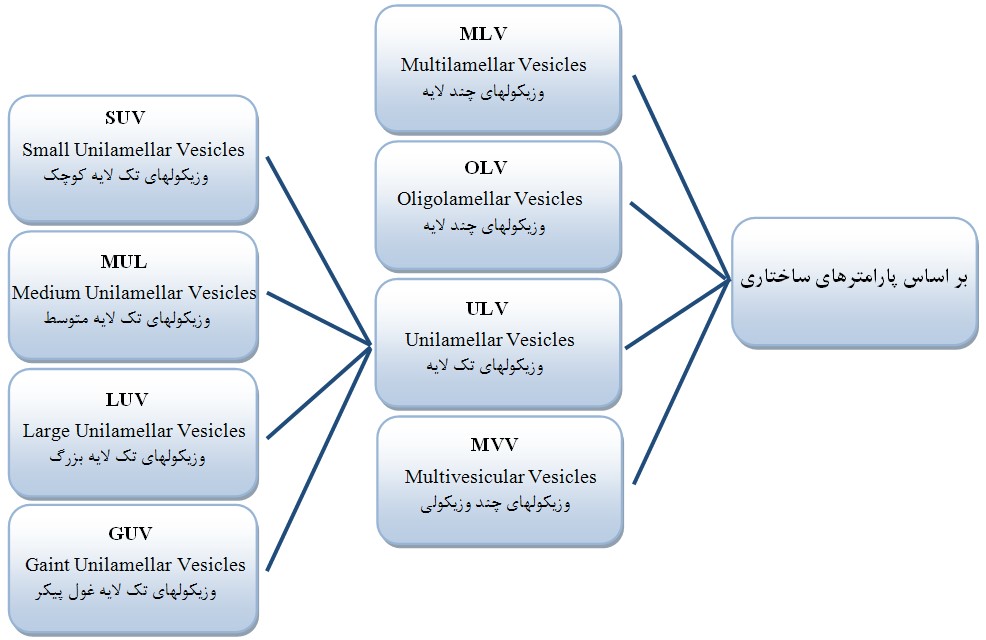 شکل-4. تقسیمبندی لیپوزومها بر اساس تعداد لایهها و اندازه آنها
شکل-4. تقسیمبندی لیپوزومها بر اساس تعداد لایهها و اندازه آنها
- فرق لیپوزوم چند دیواره (Multilamellar) و دو دیواره (Oligolamellar) در تعداد لایهها است. در لیپوزومهای چند دیواره تعداد لایههای بیشتری دیده میشود.
جدول-3. تقسیم بندی انواع لیپوزومها بر اساس ساختار و اندازه
| تعداد لایه | اندازه | انواع لیپوزوم |
| تک لایه | 20 nm – 100 nm | وزیکولهای تک لایه کوچک (SUV) |
| تک لایه | 100 nm – 400 nm | وزیکولهای تک لایه بزرگ (LUV) |
| تک لایه | و بزرگتر 1 µm | وزیکولهای تک لایه غول پیکر (GUV) |
| چند لایه | 200 nm -3 µm | وزیکولهای چند لایه (MLV) |
| چند لایه | 200 nm -3 µm | وزیکولهای چند وزیکولی (MVV) |
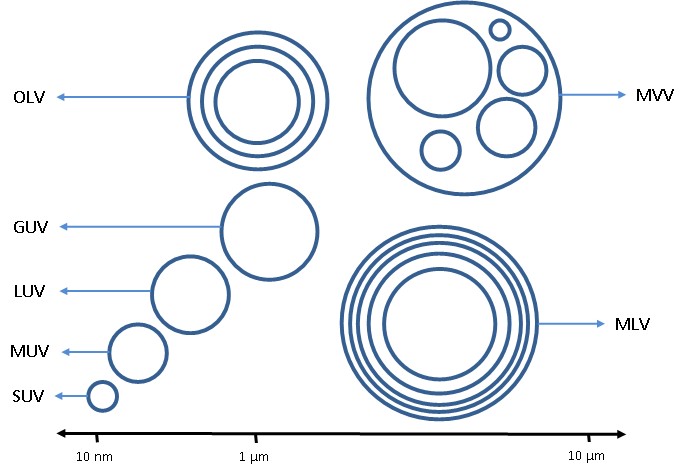 شکل- 5. دسته بندی لیپوزومها بر اساس پارامترهای ساختاری
شکل- 5. دسته بندی لیپوزومها بر اساس پارامترهای ساختاری
-
تقسیمبندی بر اساس روش تهیه لیپوزومها
جدول-4. تقسیمبندی بر اساس روش تهیه لیپوزومها
| عبارت به انگلیسی | توضیح | روشهای تهیه |
| Dehydration and Rehydration | روش آبگیری و آبدهی | DRV |
| SULs/OLVs made by reverse phase evaporation method | SUV و OLV های تهیه شده به روش فاز بخار معکوس | REV |
| MLV made by reverse phase evaporation method | MLV های تهیه شده به روش فاز بخار معکوس | MLV-REV |
| Vesicles prepared by Extrusion Technique | وزیکولهای تهیه شده یه روش انفصال | VET |
| Frozen and thawed MLV | انجماد و ذوب MLV | FATMLV |
| Stable plurilamellar vesicles | وزیکولهای چند لایه پایدار | SPLV |
4- کاربرد لیپوزوم در پزشکی و اهمیت آن در دارورسانی
درمان مسمومیتهای حاصل از فلزات سنگین از طریق شلاته دادن، جابجایی آنزیم، تصویربرداری تشخیصی از تومورها، مواد آرایشی، مطالعه غشاها و انتقال هدفمند دارو و رهایش آن از کاربردهای لیپوزومها است. لیپوزومها در انتقال داروهای ضدسرطان مانند دوکسوروبیسین[8] و سینپلاتین[9] ، باکتریکشها مانند آمپیسیلین[10]، ریفامایسین[11]، ضدویروسها، ضدقارچها مانند آمفوتریسین-بی[12]، آنزیمها مانند گلوگوزیداز و واکسنها مانند آنتیژنهای هپاتیت-بی استفاده شدهاند. لیپوزومها توانستهاند سبب کاهش اثرات نامطلوب جانبی و افزایش پایداری داروها شوند. مثلاً داروی ضد سرطان دوکسیل را به جای 20 دقیقه 50 ساعت در خون حفظ کنند. با این وجود توسعه تحقیقات بر روی لیپوزومها به دلیل مسائلی چون بازده پایین کپسوله کردن دارو، نشت سریع داروهای محلول در آب در حضور اجزاء خون، پایداری ذخیره ای کم، اثرات نامطلوب جدید و هزینه بالا محدود شده است.
کاربردهای لیپوزومها به عنوان حاملهای دارویی، شامل رسانش مواد زیر است:
- آنزیمها
- داروهای ضد سرطان
- قارچکشها
- داروهای ضد انگلی
- داروهای ضد ویروسی
- داروهای ضد باکتریایی
- انواع نوکلئیک اسیدها در دستکاریهای ژنتیکی
4-1- دارو و کپسوله کردن DNA
گسترش زیستشناسی مولکولی در دهههای اخیر روشهای جدیدی را برای درمان بیماریهای انسان ایجاد کرده است. با توجه به شناخت درونسلولی و شیوههای انتقال و تحویل ترکیبات به یک مکان معلوم، به نظر میرسد با رشد دانش شناخت نقصها و تغییرات ژنی، واسطهها در سطح ژنتیکی قابل درمان باشند. کپسوله کردن DNA با یک کپسول غشائی تک لایهای (لیپوزوم) یک راهکار کنونی است تا محتویات آن از تغییرات متابولیسم بیمار دور نگه داشته شود.
لیپوزومها ساختمانی شبیه به ذرات ویروس مانند [13](PLV) دارند که توسط میکروسکوپ الکترونی قابل مشاهدهاند. با افزودن مولکولهای خاصی برای محافظت تکلایهها میتوان وظایف خاصی مانند انتقال به یک مکان خاص را به سامانههای انتقال محول نمود.
بنابراین یک سامانه انتقال که شامل مولکولهای خاص است فقط توسط سلولهایی جذب میگردد که میتوانند آن مولکولها را جذب کنند.
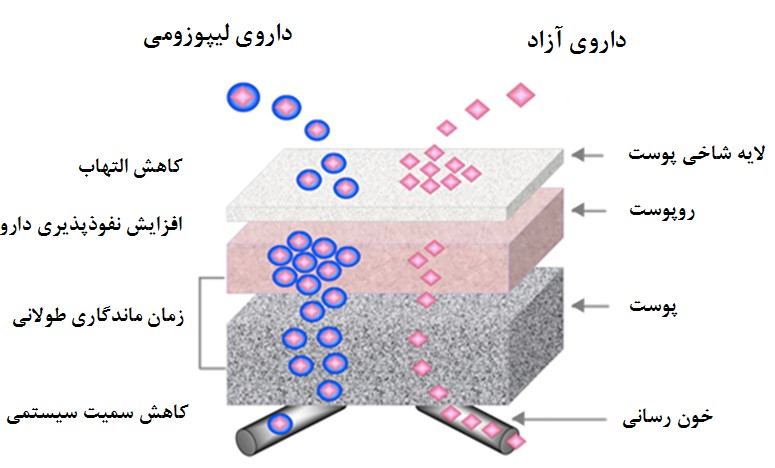 شکل- 6. نقش لیپوزوم در دارورسانی
شکل- 6. نقش لیپوزوم در دارورسانی
4-2- مزایا و معایب لیپوزومها
مزایا:
- به دام انداخته شدن فیزیکی دارو که سبب میشود جایگاه اثر دارو تغییری پیدا نکند
- گنجایش بارگیری بالای دارو و عدم تاثیر بر ویژگیهای کلی حامل دارو
- دارو در درون این حاملهای لیپوزومی از گزند تجزیه آنزیمی در امان میماند
- هم داروهای محلول در آب و هم داروهای محلول در چربی را میتواند حمل کند
- حاملهای لیپوزومی زیست فرسایشی و غیر سمی میباشند
- لیپوزومها میتوانند به اشکال سوسپانسیون، ائروسل، نیمه جامد و پودر درآیند
معایب:
- نمیتواند از سد پوششی داخلی[14] عبور کند، در نتیجه در به بافت رسیدن دارای مشکل است
- توسط سیستم شبکهای پوشش داخلی[15] بدن به عنوان ذره خارجی شناخته و بلعیده میشود [16]
- رهایش دارویی آهستهای دارند که این امر در مورد داروهای ضدسرطان با چالش رو به رو است، زیرا باعث مقاومت دارویی میشود
- قیمت تولید لیپوزومها بسیار بالا است
- نیمه عمر کوتاهی دارند
- تنها تعداد کمی از آنها پایدار هستند
5- شرکتهای مهم و پیشگام
5-1- برنامه نانوفناوري ليپوزوم پايدار پروتئيني (PSL) از Azaya
نانوفناوري PSL از شركت Azaya از نسل جديد نانوفناوري در كپسوله كردن محصولات دارويي در درون ليپوزوم استفاده ميكند. اين فناوري يك پيشرفت كليدي در حوزهي دارورساني ليپوزومي محسوب ميشود، كه با استفاده از روش توليد تك مرحلهاي ذرات يك شكل كوچكتر از 200 نانومتر را ميسازد در حاليكه تركيب داروي كپسوله شده نيز پايدار ميماند.
Azaya از يك شناورکننده[17] با فشار بالا براي هموژنيزه و يكنواخت كردن فازهاي آب و روغن استفاده ميكند. به مرور زمان، امولسيون تمايل دارد تا به حالت پايدار قبلي كه آب و روغن جدا هستند بازگردد. مواد فعال موجود در سطح يا سورفاكتانتها ميتوانند با افزايش پايداري جنبشي[18] در امولسيون، باعث شوند تا به محض تشكيل شدن آن در مدتي محدود تغيير شكلي محسوس پيدا نكنند. ليپوزوم پايدار شده بوسيله پروتئين نيز از چنين اصولي استفاده ميكند (با استفاده از آلبومين سرم انساني HAS به عنوان سورفاكتانت).
نانو فناوري PSL از شركت Azaya از اصل متفاوتي براي ساخت ليپوزومها استفاده مي كند. به جاي تغيير اندازه ليپوزومها پس از افزودن دارو به آنها، ليپوزومها طي روند هموژنيزاسيون در يك شناورکننده توليد ميشوند. در اين روش نيز از تمام اصولي كه قبلاً به آن اشاره شد استفاده ميشود.
5-2- دارورساني مبتني بر ليپوزوم از Liplasomepharma
فناوري رساندن دارو و پيشدارو مبتني بر استفاده از نانو ناقلهاي هوشمند برپايهي ليپيد به نام (Liplasome) كه در انحصار شركت Liplasomepharma ميباشد، ميتواند در انتقال هدفمند داروهاي ضد سرطان به كار رود. چگونگي طراحي نانو ناقل ليپيدي حاوي دارو به ترتيبي است كه تمايل به تجزيه شدن در حضور فسفوليپاز A2(PLA2) را دارد. اين آنزيم در محيط بافت تومورال برخي از انواع سرطان (مانند سرطان هپاتوسلولار، كولوركتال، پروستات، معده، پانكراس و سينه) افزايش نشان ميدهد.
روش خلاق رساندن دارو و پيشدارو از Liplasomepharma امكان جابجايي غلظتهاي بالاي داروهاي ضد سرطان را از طريق وريدها به سلول تومورال هدف ميدهد. با استفاده از اين روش حتي ممكن است بدون داشتن دانش قبلي در مورد محل و اندازهي تومور، داروهاي ضد سرطان را اختصاصاً در محل تومور آزاد ساخت.
روش دارورساني Liplasome شامل موارد زير ميباشد:
- سيستم دارورساني مبتني بر ليپيد (Liplasome) براي انتقال وريدي پيشداروها و داروهاي ضدسرطان در ساختار اين سيستم دارورساني از پلي اتيلين گليكول (PEG) براي طولاني ساختن نيمه عمر داروها و پيشداروها استفاده شده كه در عين حال مانع از پاك شدن نانوناقلها توسط RES[19] ميشود.
- وجود مكانيسم فعال سازي آزاد كردن دارو، براي تضمين آزاد شدن داروها و پيشداروها كه اختصاصاً در محل تومور باشد.
- بازار جهانی و محصولات
جدول 5 برخی از داروهای ترکیبی با لیپوزومها را نشان میدهد، این داروها در درون لیپوزومها انکپسوله شده اند، و با استفاده از این سیستم دارورسانی نوین لیپوزومی، راندمان اثر داروها افزایش پیدا کرده است.
جدول- 5. فهرست برخی از داروهای لیپوزومال
| کاربرد | شرکت | نام تجاری | نام دارو | |
| عفونتهای قارچی | Enzon
|
Abelcet | آمفوتریسین B لیپوزومی
Liposomal Amphotericin B |
|
| عفونتهای قارچی و آغازیان تک سلولی | Gilead Sciences | Ambisome | آمفوتریسین B لیپوزومی
Liposomal Amphotericin B |
|
| عفونتهای قارچی و آغازیان تک سلولی | اکسیر نانوسینا | SinaAmpholish | آمفوتریسین B لیپوزومی
Liposomal Amphotericin B |
|
| مننژیت دارای بافت لنفی بدخیم | Pacira (formerly SkyePharma) | Depocyt | سیترابین لیپوزومی
Liposomal Cytarabine |
|
| سارکومای کاپوسی مرتبط با HIV | Gilead Sciences | DaunoXome | دااونوروبیسین لیپوزومی
Liposomal Daunorubicin |
|
| درمان ترکیبی با سیکلوفسفامید در سرطان سینه متاستاتیک | Zeneus | Myocet | دوکسوروبیسین لیپوزومی
Liposomal Doxorubicin |
|
| هپاتیت A | Berna Biotech | Epaxal | واکسن IRIV لیپوزومی
Liposomal IRIV vaccine |
|
| آنفلوآنزا | Berna Biotech | Inflexal V | واکسن IRIV لیپوزومی
Liposomal IRIV vaccine |
|
| بی حسی بعد جراحی | SkyePharma, Endo | DepoDur | مورفین لیپوزومی
Liposomal morphine |
|
| تباهی لکه زرد چشم مرتبط با سن، بیماری میوپیای پاتولوژیک و بیماری هیستوپلاسموز چشمی | QLT, Novartis | Visudyne | ورته پورفین لیپوزومی
Liposomal verteporfin |
|
| سارکومای کاپوسی مرتبط با HIV، سرطان سینه متاستاتیک، سرطان تخمدان متاستاتیک | Ortho Biotech, Schering Plough | Doxil/Caelyx | دوکسوروبیسین لیپوزومPEG دار
Liposome-PEG doxorubicin |
|
| سارکومای کاپوسی مرتبط با HIV، سرطان سینه متاستاتیک، سرطان تخمدان متاستاتیک | اکسیر نانوسینا | SinaDoxoSome | دوکسوروبیسین لیپوزومال
Liposomal doxorubicin |
|
| درمان یائسگی | Novavax | Estrasorb | میسلار استرادیول
Micellular estradiol |
|
| خاصیت آنتی اکسیدانی، ضد التهاب و میکروب کش | MaxHealthLabs
|
CURCUMIN Cu(II) | کورکومین لیپوزومال
Liposomal Curcumin |
|
6-1– پيشبيني و نماي كلي بازار
طبق گزارش انجام شده توسط Dewan، حجم بازار جهانی دارورسانی هدفمند در سال 2011، 92.1 بیلیون دلار بوده است. بیشترین حجم این بازار مربوط به بخش نانوذرات بوده است. حجم بازار جهانی لیپوزومها و نانوذرات، در سال 2013 به ترتیب حدود 1.2 بیلیون دلار و 53 بیلیون دلار بوده است. انتظار میرود این بازار در سال 2018 با رشد 2.4 درصدی به رقم 109 بیلیون دلار برسد. اين موضوع ناشي از ميزان هزينههاي بالايي است كه صرف تحقيق و توسعه وابسته به نانوفناوري در صنايع داروسازي و بخش سلامت ميشود. توسعه بازار نانو ذرات به واسطه پیشرفت داروهای نانوفناوری در سرطان است، که اثرات جانبی را به طور موثری کاهش می دهد (Dewan, 2014).
جدول- 6 . بازده جهانی سامانه رهایش دارو به واسطه لیپوزومها، تا سال 2018 (میلیون دلار)
| CAGR%
2018-2013 |
2018 | 2013 | 2012 | 2011 | سیستم |
| 4.5 | 1.493.3 | 1.198.6 | 1.111.4 | 1.076.8 | لیپوزوم |
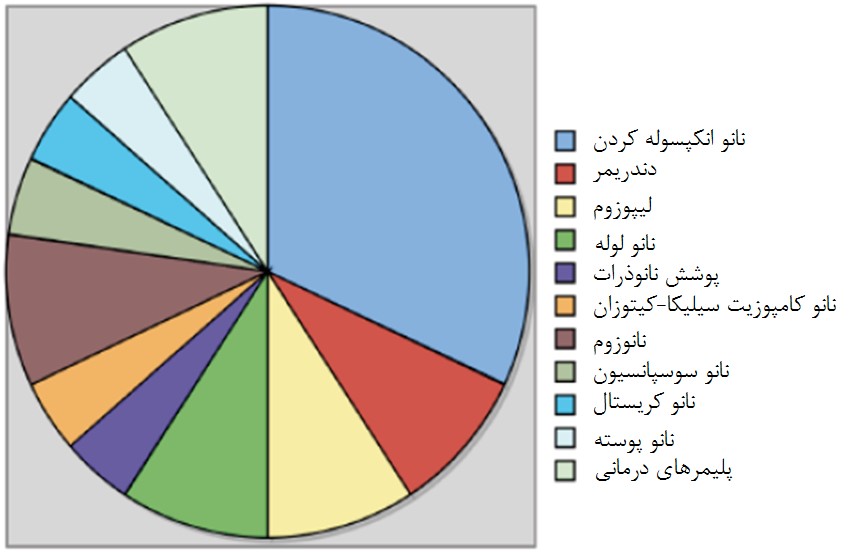 شکل- 7. تفکیک سیستم دارورسانی نانوذرهای بر اساس فناوری
شکل- 7. تفکیک سیستم دارورسانی نانوذرهای بر اساس فناوری
—————————–
پانوشت:
[1] Vesicle
[3]Encapsulatian
[4]myelin
[5]ammonium oleat
[6]self-assemble
[7]entrapping
[8] Doxorubicin
[9]Cinpelatin
[11] rifamycin
[12]Amphotericin B
[13] Particle like virus
[14] endothelial
[17] fluidizer
[18] kinetic stability
[19] reticuloendothelial system
————————————–
6-2- وضعیت فناوری در ایران
مطالعـات و تحقیقـات زیـادی در زمینـه اسـتفاده از نانولیپوزومها در کشـور مـا صـورت پذیرفتـه اسـت. ایـن مطالعـات بـا هـدف ایجـاد و توسـعه فنـاوری نانـو و اصـلاح محصـولات نانـو در سـطوح مختلــف در مراکــز تحقیقاتــی و دانشــگاهی ایــران مــورد بررســی و کنــکاش قــرار گرفتــه اســت. از مجموعه فعالیتهای انجام شده، موارد زیر قابل اشاره هستند:
جدول-7. وضعیت فناوری نانولیپوزومها در ایران
———————————–
منابع و مراجع
- سایت آموزش فناوری نانو (nano.ir)
- سایت ستاد ویژه توسعه فناوری نانو، بانک اطلاعاتی فناوری نانو (irannano.ir)
- گزارش پیمایش فناوری و بازار حوزه نانودارورسانی، آگوست 2007
- نانوفناوری مولکولی و نانوفناوری زیستی: تعاملی بین طبیعت و فناوری، 1386، جهانشاهی م. انتشارات دانشگاه مازندران
- Bangham, A.D., Liposomes: realizing their promise. 1992, Hosp Pract (Off Ed). 27(12): 51-6, 61-2
- Bernard, A.T., A. Roum, and D. Pathol, 1947. Exper, 14, 53
- Mozafari M.R., Flanagan J., Matia-Merino L., Awati A., Omri A., Suntres Z.E. and Singh H., 2006. Recent trends in the lipid-basednanoencapsulation of antioxidants and theirrole infoods. Journal of the Science of Food and Agriculture. 86: 2038–2045
- Mozafari M.R., Khosravi-Darani K., Borazan G.G., Cui J., Pardakhty A. and Yurdugul S., 2008. ENCAPSULATION OF FOOD INGREDIENTS USING NANOLIPOSOME TECHNOLOGY. International Journal of Food Properties. 11: 833–844
- Shalini Shahani January 2014. PHM006J – Global Markets and Technologies for Advanced Drug Delivery Systems. Bcc Research GLOBAL MARKETS AND TECHNOLOG
- Zasadzinski J.A., Wong B., Forbes N., Braun G. and Wu G., 2011. Novel methods of enhanced retention in and rapid, targeted release from liposomes. Current opinion in colloid & interface science 16(3): 203-214
———————————————————————
بخش ترویج صنعتی فناوری های نانو و میکرو
====================================================================================
[جهت دسترسی به گزارش نهایی محصولات و شرکتهای دارای گواهی نانومقیاس ستاد توسعه فناوریهای نانو و میکرو به «کتب مرجع محصولات و تجهیزات نانو و صنعت» به نشانی (INDnano.ir/category/book) مراجعه کنید]
[همچنین برای دسترسی به فایل PDF کلیه گزارشات بهمراه جزئیات، به بخش گزارش های صنعتی پایگاه اینترنتی رسانه تخصصی نانو و صنعت (www.INDnano.ir/category/report) مراجعه نمایید]
====================================================================================