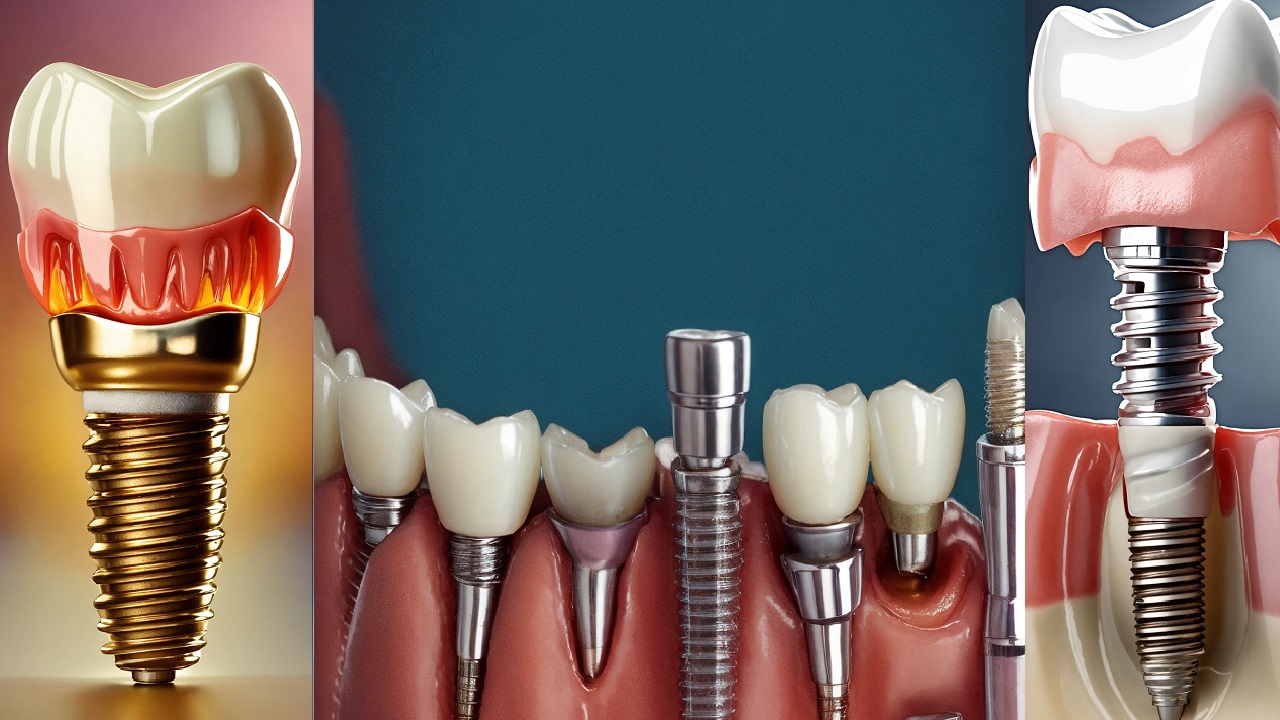
نرخ استفاده از پروتزهای زانو و لگن در طی ده سال گذشته در بیشتر کشورهای جهان به علت بالا رفتن میانگین سنی جمعیت و همچنین افزایش اعتماد به روشهای عملهای جراحی ارتوپدی برای تعویض مفاصل، افزایش پیدا کرده است. از آنجا که متوسط طول عمر مواد کاشتنی استخوانی کمتر از 15 سال است، به زیست مواد با کیفیتتر ارتوپدی نیاز است. استفاده از فناوری نانو در حوزه تولید پروتزها و ایمپلنتهای ارتوپدی، سبب افزایش طول عمر و بهبود کیفیت این محصولات خواهد شد. در این گزارش به بررسی پایه و مبانی کلی پروتزها، ایمپلنتهای ارتوپدی و چالشها و مشکلات آنها پرداخته میشود. در انتها به نمونههای تجاری بعضی از ایمپلنتها و شرکتهای فعال در این زمینه اشاره خواهد شد.
مقدمه
صنعت ایمپلنتهای ارتوپدی در حال تجربه یک رشد سریع است. طبق گزارش آژانس تحقیقات و کیفیت بهداشت، هر ساله بیش از 450،000 تعویض مفصل لگن در ایالاتمتحده انجام میشود که البته تمام این عملهای جراحی موفقیتآمیز نیستند و نیاز به جراحی مجدد پیدا میکنند. مشکل تعویض مفاصل روزبهروز افزایش مییابد، بنابراین فناوری میبایست در این زمینه نقش خود را ایفا کند و روشهای قدیمی را بهروزرسانی و سازگارتر کند. یکی از رایجترین بیماریهای تخریبی، پوکی استخوان است که 6/9 درصد از مردان و 18 درصد از زنان در بالای سن 60 سالگی در جهان به آن دچار میشوند. اگرچه افزایش سن یکی از فاکتورهای مهم به شمار میآید اما این پدیده در بیماران جوانتر نیز به علت دلایلی مانند تصادفات و حوادث در حال رایج شدن است.
نرخ استفاده از پروتزهای زانو و لگن در طی ده سال گذشته در بیشتر کشورهای جهان به علت بالا رفتن میانگین سنی جمعیت و همچنین افزایش اعتماد به روشهای عملهای جراحی ارتوپدی برای تعویض مفاصل، افزایش پیدا کرده است. در حال حاضر تعویض مفاصل لگن و زانو بهترین و مؤثرترین روش برای از بین بردن آرتروز، کاهش درد و بازیابی حرکتی بیمار و برگشت به زندگی عادی است. یک عمل معمولی تعویض مفصل با هدف کاهش درد و بازیابی حرکت بیمار و برگشت عملکرد مفصل به حالت عادی انجام میپذیرد.
از دیگر مشکلاتی که بیشتر افراد سالخورده با آن مواجه هستند کمردرد است که در حالت تشدید شده، نتیجه آن عمل جایگزینی دیسک و یا مهرهٔ از بین رفته در ناحیه گردنی و کمری ستون فقرات است. در واقع تخریب دیسک یک فرایند طبیعی است که با افزایش سن رخ میدهد و موجب تغییراتی در شکل ظاهری و ساختار شیمیایی دیسک میشود، این تغییرات زیستی موجب تخریب دیسک و کمردرد میشود. در تخریبهای خفیف که تنها قسمتی از دیسک آسیبدیده است، روشهای مستقل از جراحی مانند انواع ثابتکنندههای خارجی مورد استفاده قرار میگیرد. روشهای وابسته به جراحی شامل سه گروه فیوژن[1]، جایگزینی دیسک و پایدار کنندههای حرکتی است. در روش فیوژن از کیجها[2] به منظور جایگزین کردن آن با دیسک بین مهرهای استفاده میشود، این کیجها غالباً از دو جنس پیک[3] و تیتانیوم هستند [1]. در این گزارش تمرکز اصلی روی فناوریهای مورد استفاده در پروتزهای زانو و لگن و ایمپلنتهای ستون فقرات و لزوم بهکارگیری و بهرهمندی از فناوری نانو در راستای بهبود خواص این کاشتنیهای درونتن است و در انتها بازار و صنعت کاشتنیهای ارتوپدی نانو محور، مورد بررسی قرار خواهد گرفت.
شرکتهای برتر تولیدکننده محصولات ارتوپدی در جهان
هر ساله شرکتهای تولیدکننده محصولات ارتوپدی بر اساس گزارش سالانه فروش محصولات خود طبقهبندی میشوند [2]. در جدول ۱ میزان فروش ده شرکت برتر در حوزه ارتوپدی در سال 2019 آورده شده است. مجموع فروش این شرکتها بالای 40 میلیارد دلار در سال است و هر ساله این غولهای صنعت ارتوپدی سرمایهگذاری بسیاری در خرید محصولات و یا برند شرکتهای کوچک، موفق و فناور میکنند.
جدول 1- ده شرکت برتر جهانی تولیدکننده پروتزهای ارتوپدی در سال 2019 [2]
| رتبه | نام شرکت | میزان فروش |
| 1 | Stryker | $13.60B |
| 2 | DePuy Synthes | $8.88B |
| 3 | Zimmer Biomet | $7.93B |
| 4 | Smith & Nephew | $4.90B |
| 5 | Medtronic Spine | $2.65B |
| 6 | NuVasive | $1.10B |
| 7 | Wright Medical | $836M |
| 8 | Globus Medical | $713M |
| 9 | Össur | $613M |
| 10 | Integra LifeSciences | $509M |
آناتومی سطوح مفصلی و مبانی کلی پروتزهای تعویض مفاصل
مفصل در واقع یک ارتباطدهنده است که بین استخوانهای بدن ایجاد میشود و سیستم اسکلتی را به یک کل عملکردی متصل میکند؛ آنها ساخته شدهاند تا درجات و انواع مختلف حرکت را امکانپذیر کنند. بعضی از مفاصل مانند زانو، آرنج و شانه خودروانکننده و تقریباً بدون اصطکاک هستند و در عین انجام حرکات صاف و دقیق، قادر به مقاومت در برابر فشار و حفظ بارهای سنگین هستند. سطح مفصل توسط یک سطح صاف پوشانده شده است که امکان حرکت بدون درد در مفصل را فراهم میکند. در واقع غضروف روی مفاصل قرار میگیرد و اجازه میدهد استخوانها حرکت نرم داشته باشند (شکل 1). زانو بزرگترین مفصل بدن انسان است و ران را به ساق پا پیوند میدهد. ساختار کلی زانو تا حدی ناپایدار است. با این وجود زانو باید کل وزن بدن را هنگام ایستادن تحمل کند و هنگام راه رفتن یا دویدن حتی وزن بیشتری به آن تحمیل میشود؛ بنابراین مشکلات زانو از جمله بیماریهای بسیار شایع در همه سنین است. در شکل 1 اجزای مختلف مفصل زانو و در شکل 3 اجزای مختلف مفصل ران قابل مشاهده است.
شکل 1- سطح مفصلی (غضروفی) در زانو
شکل 2- زانوی راست از نمای راست [3]
شکل 3- اجزای مفصل ران
سطوح مفصلی به دلایل مختلف و نامعلومی میتوانند دچار فرسودگی و سایش شوند که در حال حاضر دلیل علمی آن نامشخص است. هنگامیکه غضروف مفصل فرسوده میشود، انتهای استخوان روی یکدیگر مالیده و باعث درد میشود. آرتروز اصطلاح عمومی است که شرایط مختلفی را که در آن سطح مفصل (غضروف) فرسوده میشود را شامل میشود. یکی از روشهای درمان آرتروز در حالتی که بیمار دچار درد شدید شده باشد و یا در اثر جراحت بخش قابل توجهی از مفصل خود را از دست داده باشد (شکل 4)، جایگزینی کامل مفصل[4] (TJR) است که برای از بین بردن درد و بازیابی حرکت مفصل، تمام یا بخشی از مفصل را با یک دستگاه مصنوعی (پروتز) جایگزین میکنند (شکل 5 و شکل 6). امروزه طول عمر پروتزهای ارتوپدی مانند پروتزهای مفصل ران و زانو تقریباً 10 تا 15 سال است. با این حال، با توجه به افزایش جمعیت و افزایش تقاضا برای جراحی ارتوپدی حتی در بیماران جوان، ایمپلنتها باید بیش از 30 سال عمر داشته باشند. در پروتزهای مصنوعی جزئی که در واقع کارکرد غضروف را شبیهسازی میکند همان جزء پلیمری (Plastic spacer) در شکل 5 و یا (Plastic liner) در شکل 6 است. لازم به ذکر است که این تعدد نامگذاری سلیقهای است اما به طور کلی به این جزء لاینر گفته میشود. بنابراین از آنجایی که این جزء کارکرد غضروف را شبیهسازی میکند باید خواص فیزیکی و شیمیایی مانند خواص روغنکاری، مقاومت به ضربه و سایش داشته باشد. به همین دلیل یکی از مواد پلیمری مناسب در این زمینه پلیاتیلن است. البته طبق تحقیقات صورت پذیرفته سایش جزء پلیمری مهمترین دلیل عدم موفقیت عملهای جراحی است که دلیل آن، محصولات ناشی از سایش پلیاتیلن است که در هنگام کاشت در درون بدن شکل میگیرند و با یک واکنش التهابی، تشکیل یک غشای سست و خورده شدن ثانویه استخوان آغاز میشود، بنابراین جلوگیری و یا به تعویق انداختن تخریب جزء پلیاتیلنی پروتزهای تعویض زانو و لگن باعث نجات زندگی و همچنین افزایش امید به زندگی میشود. به همین دلیل بحث بهبود خواص پلیاتیلن در تمام نقاط جهان بسیار حائز اهمیت است.
شکل 4- در تعویض کامل زانو، استخوان و غضروف آسیبدیده برداشته شده و با اجزای فلزی و پلیمری جایگزین میشود که سطح مفصل را بازسازی میکند[4]
شکل 5- اجزای پروتز تعویض کامل مفصل زانو [4]-
شکل 6- اجزای پروتز تعویض کامل مفصل ران [5]-
آناتومی ستون فقرات و آشنایی با کیجهای ستون فقرات
ستون فقرات از 33 مهره تشکیل شده است. این مهرهها توسط رباطها و ماهیچهها به یکدیگر متصل هستند و یک حالت S شکل را به ستون فقرات میدهند. بین هر کدام از مهرهها دیسک بین مهرهای قرار میگیرد. دیسک بین مهرهای یک ماده ژلاتینی نسبتاً نرم است که فشارهای وارد شده روی مهرهها را به طور یکنواخت پخش و حرکت مهرهها را روی یکدیگر آسان میکند و باعث خم و راست شدن یا چرخش کمر میشود. یک حرکت سریع و یا برداشتن اجسام سنگین ممکن است باعث آسیب به این ناحیه و فتق دیسک بین مهرهای شود. فتق دیسک اغلب به طرف پشت، چپ و راست اتفاق میافتد و باعث انتشار درد در پا یا دست همان طرف که فتق دیسک رخ داده میشود (شکل 7).
شکل 7- شماتیک نحوه قرارگیری مهرهها و دیسک بین مهرهای
برای درمان دیسک کمر (فتق دیسک) حتماً باید مایع بین مهرهای (دیسک) خارج شود و به جای آن کیج قرار داده شود. کیجها انواع مختلفی دارند که بر اساس تشخیص پزشک جراح استفاده میشوند (شکل 8). از آنجایی که این کیجها عمدتاً از پلیمر PEEK ساخته شدهاند و با توجه به خواص ذاتی و مدول این پلیمر، متأسفانه تناسب زیادی با خواص فیزیکی و شیمایی استخوانهای مهره کمری ندارند؛ بنابراین باعث میشود که انسجام و اتصال مطلوبی در آن ناحیه برقرار نشود و از طرفی این پلیمر خواص زیست فعالی خوبی برای ایجاد یک پیوند قوی استخوانی ندارد؛ بنابراین مطالعات وسیعی برای استفاده از مواد نانویی مختلف برای بهبود خواص این کیجها در حال انجام است.
در ادامه گزارش، دو ماده رایج مورد استفاده در کاشتنیهای ارتوپدی یعنی هیدروکسی آپاتیت (به عنوان جایگزین استخوان طبیعی) و پلیاتیلن (به عنوان سطوح مفصلی) بررسی میشوند. مزایا و نمونههای تجاری این دو ماده نیز بررسی خواهد شد.
شکل 8- نحوه قرارگیری کیج در بین مهرههای گردن/کمر.
هیدروکسی آپاتیت (HA)
هیدروکسی آپاتیت (HA) به دلیل شباهت آن به ساختار معدنی به طور گستردهای به عنوان سرامیک زیست سازگار در بسیاری از زمینههای پزشکی مورد استفاده قرار گرفته است؛ اما عمدتاً برای تماس با بافت استخوان است. در پستانداران، اسکلت استخوانی شامل آپاتیت کربناته و تا حدی آپاتیت جایگزین[5] شده است که بر اساس تجمع نانوکریستالهای آن و همراه شدن آنها با کلاژن، ساختارهای سهبعدی موجود در ساختارهای مختلف بافت استخوانی مانند استخوان قشری یا اسفنجی را ایجاد میکند [6].
پلیاتیلن و انواع آن
پلیاتیلن یکی از انواع پلیمرها است که از گاز اتیلن (C2H4) با وزن مولکولی 28 تشکیل شده است. فرمول کلی شیمیایی پلیاتیلن -n(C2H4)- است؛ که n درجه پلیمریزاسیون آن است [7].
شکل 9- شماتیک ساختار شیمیایی پلیاتیلن [8]
بهصورت عملی در صنعت، پلیمرها توسط مونومرهای دیگر، کوپلیمر میشوند، (مانند پلیپروپیلن) که این عمل برای به دست آوردن خواص فرایندی بهتر و همچنین تغییر در خواص فیزیکی و مکانیکی انجام میشود.
پلیاتیلن انواع مختلفی دارد که به شرح زیر است:
:LDPE[6] پلیاتیلن با دانسیته پایین
LLDPE[7]: پلیاتیلن سبک خطی
:HDPE[8] پلیاتیلن با دانسیته بالا
: UHMWPE[9]پلیاتیلن با وزن مولکولی بسیار بالا
این پلیمرها توسط وزنهای مولکولی متفاوت و ساختارهای متفاوت سنتز میشوند. HDPE یک پلیاتیلن خطی با وزن مولکولی تا g/mol 200000 است در حالی که UHMWPE دارای متوسط وزن 6000000 g/mol است [9].
پلیمر پلیاتیلن با وزن مولکولی بسیار بالا، یک پلیمر ویژه است که خواص فیزیکی و شیمیایی برجستهای دارد. از مهمترین خواص آن میتوان خنثی بودن، خاصیت روان کاری، استحکام در مقابل ضربه و استحکام سایشی را نام برد. حدوداً 50 سال است که از این پلیمر در ارتوپدی استفاده میشود. سالانه حدود 3 میلیون عمل تعویض مفصل در جهان انجام میشود که بیشتر آنها توسط این پلیمر انجام شده است.
در واقع میتوان زنجیره مولکولی UHMWPE را مانند یک رشته ماکارانی در هم رفته به طول یک کیلومتر تصور کرد، زیرا زنجیره آن ایستا نیست و دارای انرژی درونی (حرارتی) است و زنجیره مولکولی در دماهای بالا متحرک میشود (شکل 10).
شکل 10- مورفولوژی UHMWPE [10]
استفاده از UHMWPE به عنوان مفاصل مصنوعی تقریباً از سال 1962 توسط سر جان چارلی[10] زمانی که اولین پروتز لگن را استفاده کرد، شروع شد. از آن تاریخ به بعد UHMWPE به عنوان ماده انتخابی در عملهای تعویض مفاصل مورد استفاده قرار گرفت و همانطور که ذکر شد علیرغم موفقیتهای خارقالعاده این کاشتنی، سایش اجزای آن و در نتیجه عفونت و شل شدن این پروتزها باعث یکسری مشکلات میشوند که طول عمر استفاده از این کاشتنی را محدود به 15 الی 20 سال میکند.
طبق ISO 11542 که استاندارد صنعتی برای UHMWPE است، این پلیمر میتواند شامل غلظت بالایی از کوپلیمر (تا 50%) باشد و همچنان بهعنوان UHMWPE نامیده شود. پلیمرهای UHMWPE که در ارتوپدی استفاده میشوند هموپلیمر هستند. ویژگی اصلی پلیمر که آن را از دیگر مواد مانند فلز و سرامیک متمایز میکند اندازه مولکولی آن است. در آلیاژهای فلزی و سرامیکی بلوکهای ساختمانی عنصر به صورت تک اتم فلزی است مانند (Cr،Co)، یا مولکولهای نسبتاً کوچک (مانند فلزات کاربیدی یا اکسیدی). درحالیکه در یک پلیمر، اندازه مولکولی میتواند به صد هزار واحد مونومری با وزن مولکولی چند میلیون گرم بر مولکول برسد لذا با تغییر وزن مولکولی و یا انتخاب مواد با وزن مولکولی دلخواه میتوان به خواص دلخواه دست پیدا کرد [11].
علیرغم ویژگیهای منحصربهفردی که این پلیمر دارد، طول عمر آن محدود است که البته یکی از روشهایی که به صورت تجاری برای بهبود طول عمر این پلیمر استفاده میشود ایجاد پیوند عرضی[11] توسط اشعه گاما است. البته این روش درست است که خواص بهتری را نسبت به UHMWPE خالص نشان میدهد اما کماکان از نظر طول عمر فاصله زیادی با ایدهآلهای پزشکی دارد [11].
شکل 11- پودر UHMWPE
یکی از بزرگترین تولیدکنندگان پودر UHMWPE با درجه پزشکی، شرکت CELANESE آلمان است که این پودرها را با نشان تجاری GUR[12] تولید میکند (شکل 11).
به طور مثال محصول تجاری ® Prolong در حال حاضر توسط شرکت Zimmer به بازار عرضه شده است که همان پلیاتیلن پیوند عرضی داده[13] شده است. در ادامه مقالات و متون علمی که از فناوری نانو در بهبود خواص این پروتزها استفاده شده است، مورد بررسی قرار خواهد گرفت.
شکل 12- عکس انواع اشکال شکست اجزای پلیمری (A) مفصل ران، (B) شانه، (C) زانو و (D) انگشت [12]
نانولولههای کربنی
نانولولههای کربنی نسبت سطح به حجم بالایی دارند و دارای قطری حدوداً 5 الی 15 نانومتر و طولی تا 50 نانومتر هستند. ساختار تو خالی کربن توسط یک اتم با دیواره ضخیم (صفحات گرافن) شکل میگیرد. نانولولههای کربنی بر اساس ساختاری که دارند به دو گروه تک دیواره و چند دیواره تقسیم میشوند (شکل 13).
شکل 13- نانولولههای کربنی تک دیواره و چند دیواره [10]
خواص مکانیکی ذاتی کربن مانند چگالی پایین، مدول الاستیک حدود Tpa 1 و استحکام کششی نزدیک به 30 الی Gpa100، کربن را یک نماینده بسیار عالی به عنوان تقویتکننده برای پلیاتیلن معرفی میکند که البته در عمل این مقادیر بسیار کمتر هستند که دلیل آن ایجاد کلوخه به علت تجمع ذرات کربن در یک ناحیه خاص و یا عدم وجود کربن در بعضی از نواحی میتواند باشد [14]. نتایج تحقیقات نشان میدهد که استفاده از نانولولههای کربنی به عنوان تقویتکننده در UHMWPE باعث افزایش مدول یانگ میشود. تنش تسلیم در کامپوزیت MWCNT/UHMWPE تا دو برابر UHMWPE معمولی در تست فشار افزایش نشان میدهد. همچنین میزان خزش در این کامپوزیت کاهش پیدا میکند که باعث شد شرکت zimmer در محصولات خود نیز از این نانولولهها استفاده کند [14]. مقالات زیادی در زمینه استفاده از نانوذرات در راستای بهبود خواص مکانیکی و شیمیایی این پروتزها چاپ شده است که نوید امیدواری به آینده و بهبود عملکرد هر چه بیشتر این پروتزها را میدهد
[13], [15]–[19].
تاریخچه تجاری فناوری نانو در تعویض مفاصل
Poly II: Zimmer
در دهه 1970، کامپوزیتهای «تقویت شده با الیاف کربن (CFR)-UHMWPE[14]» برای استفاده ارتوپدی در نظر گرفته شد و حتی به صورت تجاری معرفی شد (Poly II: Zimmer, Inc., Warsaw, IN) (شکل 12). با این حال، شکستهای فاجعه بار بالینی کوتاهمدت که با نقص در ترکیب همراه بود، در نهایت منجر به کنار گذاشته شدن Poly II شد [20], [21]. در واقع حالتهای مختلف شکست بالینی کامپوزیتهای کربن UHMWPE با روشهای استاندارد آزمایش و تجزیهوتحلیل موجود در زمان تولید کامپوزیت، به خوبی شبیهسازی نشده بود و ارزیابیهای اولیه کامپوزیتهای CFR-UHMWPE به طور کلی نتایج دلگرمکنندهای را ارائه داده بود و چندین مطالعه نشان داده بود که خصوصیات تریبولوژیکی[15] و مکانیکی کامپوزیتهای کربن UHMWPE در مقایسه با UHMWPE خالص افزایش یافته بود.
آن چیزی که در استفاده از مواد نانو در این نوع پروتزها حائز اهمیت است رسیدن به یک ترکیب یکنواخت و همگن و همچنین ایجاد یک پیوند قوی بین فصل مشترک نانو ذرات کربن و زمینه UHMWPE است. نانوکامپوزیت مذکور در کوتاهمدت به علت عدم اتصال مناسب سطح مشترک نانوذرات با ماتریس پلیمری کارایی خود را از دست
میدهد؛ اما به صورت شگفتانگیزی تعدادی از محصولات poly II مدتزمان زیادی در بدن بیماران کارایی مطلوب از خود نشان دادند (شکل 12). در ادامه و در سالهای اخیر شرکتهای مختلفی اقدام به تولید محدود کامپوزیتهای نانولولههای کربنی UHMWPE کردهاند اما هنوز گویا راه طولانی برای تجاریسازی و تولید انبوه این کامپوزیتهای نانویی در پیش است.
شکل 14- تصویر میکروسکوپ الکترونی روبشی با بزرگنمایی 350 برابر نشاندهنده الیاف کربنی که در سطح مفصلی جزء کشککی[16] پروتز Poly II قرار دارد. از ماتریس پلیمری بیرون زده و چسبندگی ضعیفی در سطح مشترک خود با ماتریس UHMWPE دارد.
شکل 15- تصویر جزء پلیمری پروتز Poly II ساخت شرکت Zimmer که به علت ساییدگی و شل شدگی پس از 32 سال از بدن بیمار خارج شد.
محصولات تجاری شده فناوری نانو در حوزه ارتوپدی
1. ایمپلنت مهره گردنی Nano FortiCore
شکل 16- ایمپلنت مهره گردنی Nano FortiCore.
این ایمپلنت محصول شرکت Nanovis مستقر در آمریکا است که یک شرکت مبتنی بر فناوری است که ایمپلنتهای تقویت شده با سیستمهای ثابتسازی[17] را ارائه میدهد. Nanovis نمونهای از ایمپلنتهای ستون فقرات را به جراحان ستون فقرات ارائه میدهد که به اعتقاد آنها پیشرفتهترین فناوری تثبیت را ارائه میدهد [22].
ویژگیهای محصول:
- وجود نانولولههای قابلبرنامهریزی با قطر 70 نانومتر در سطح
- دارای لایه کلسیم فسفات
- داربست تیتانیومی با تخلخلهای عمیق و راه به در که به اتصال بهتر ایمپلنت با استخوان در فضای بین مهرهای کمک میکند.
- استفاده از پلیمر PEEK برای ایجاد تضاد بهتر در تصویربرداری X-Ray.
- نانوهیدروکسی آپاتیت سنتزی «BelOSTO»
این محصول ساخت شرکت Nanoapatit کشور روسیه است که هدف از تولید آن ایجاد جایگزین برای بخشی از استخوان از دست رفته (در تروماتولوژی، ارتوپدی، جراحی، دندانپزشکی) است. این محصول به دلیل سازگاری زیستی و فعالیت زیستی، ماده اصلی معدنی در تولید موادی است که بخشی از استخوان از دست رفته را جایگزین میکنند. این مواد توسط سیستم ایمنی پس زده نمیشوند و قادرند به طور فعال به بافت استخوانی سالم متصل شوند. نانو هیدروکسی آپاتیت سنتزی «BelOSTO» عمدتاً از ذرات هیدروکسی آپاتیت با اندازهای از 8 تا 10 نانومتر تشکیل شده است [23].
شکل 17- نانوهیدروکسی آپاتیت سنتزی «BelOSTO»
- فیکسچر OPRA BIOHELIX
این محصول ساخت شرکت Integrum AB کشور سوئد است. از ویژگیهای این محصول میتوان به کاهش زمان بهبودی، بهبود استحکام پیوند استخوان به ایمپلنت و افزایش میزان استخوانسازی اشاره کرد. همچنین وجود تخلخلهای میکرو و نانویی (وجود نانوذرات تیتانیومدیاکسید) در سطح و ساختار این ایمپلنت باعث بهبود اتصال استخوان با ایمپلنت و در نهایت ثبات عالی این ایمپلنت میشود.
شکل 18- فیکسچر. OPRA BIOHELIX
- NanoBone SBX Putty
بتونه نانویی استخوان SBX محصول شرکت ARTOSS GmbH آلمان است که در آن از نانوذرات هیدروکسی آپاتیت استفاده شده است. در این محصول، ترکیبی از زیست نانو[18] کاربردی برای ترمیم استخوان و سادگی استفاده توسط جراح را داریم. در واقع این محصول به عنوان یک ماده پرکننده استخوان برای استفاده در درمان نقایص استخوانی مادرزادی و یا نقص ایجاد شده توسط جراحات و تصادفات است [24].
شکل 19- بتونه نانویی استخوان SBX
——————————–
پانوشت:
[1] Fusion
[2] Cage
[3] PEEK
[4] Total Joint Replacement
[5] substituted apatite
[6] Low-density polyethylene
[7] linear low density polyethylene
[8] High density polyethylene
[9] Ultrahigh-Molecular-Weight Polyethylene
[10] Sir John Charnley
[11] cross-linked
[12] Granular UHMWPE Ruhrchemie
[13] Cross linked
[14] carbon fiber-reinforced (CFR)– UHMWPE composites
[15] tribological
[16] Pattelar
[17] fixation
نتیجهگیری و جمعبندی
در این گزارش به صورت خلاصه نمایی از بازار وسیع و پیشرفته تولید محصولات ارتوپدی مورد بررسی قرار گرفت. با توجه به مواردی که ذکر شد بدیهی است که توقع بهبودی کامل و برگشت به حالت طبیعی بدن بعد از عملهای ارتوپدی دور از انتظار است زیرا هیچگاه مواد سنتزی و مصنوعی نمیتوانند عملکرد اعضای زیستی را به صورت کامل شبیهسازی کنند. پرواضح است که هر ماده سنتزی و مصنوعی معایب و مشکلاتی را به همراه دارد. بنابراین محققان در تلاش هستند با پیشرفت علم و فناوری بتوانند هرچه بهتر توسط مواد سنتزی عملکرد اعضای بدن را شبیهسازی کنند. در حوزه ارتوپدی نیز کاربرد مواد نانو میتواند راهگشایی برای بهبود خواص این کاشتنیهای درونتن باشد. در حال حاضر هزاران مقاله در زمینه استفاده از نانوذرات در راستای بهبود خواص این کاشتنیها انجام شده است که در بحثهای آزمایشگاهی اثربخشیهای مطلوبی نیز داشتهاند. به علاوه در چند دهه اخیر شرکتهای معروفی به صورت سعی و خطا و همچنین تجاری، محصولات نانو محور را در این زمینه ارائه کردهاند که نویدبخش خوبی برای بهبود عملکرد و طول عمر این نوع کاشتنیها است.
———————————-
منابع
[1] ع. حامد, ف. محسن, and ب. ا. حمید, «شبیهسازی سهبعدی به روش اجزا محدود کیجاینفیوژن خلفی-کمری با دو ماده PEEK و تیتانیوم.» چهارمین کنفرانس ملی و دومین کنفرانس بینالمللی پژوهشهای کاربردی در مهندسی برق، مکانیک و مکاترونیک, May 11, 1396, Accessed: Jun. 11, 2021. [Online]. Available: https://civilica.com/doc/626667/certificate/print/.
[2] “The 2019 Top 10 Global Orthopedic Device Firms – Covering the specialized field of orthopedic product development and manufacturing.” https://www.odtmag.com/issues/2019-08-14/view_features/the-2019-top-10-global-orthopedic-device-firms-955005/ (accessed May 31, 2021).
[3] “Knee – Wikipedia.” https://en.wikipedia.org/wiki/Knee (accessed Jun. 02, 2021).
[4] “orthoinfo.” https://orthoinfo.aaos.org/en/treatment/knee-replacement-implants/ (accessed May 31, 2021).
[5] “The Different Types of Joint Replacement Surgeries | Advanced Bone & Joint.” https://www.advancedboneandjoint.com/the-different-types-of-joint-replacement-surgeries/ (accessed May 31, 2021).
[6] M. P. Ferraz, F. J. Monteiro, and C. M. Manuel, “Hydroxyapatite nanoparticles: A review of preparation methodologies.,” J. Appl. Biomater. Biomech., vol. 2, no. 2, pp. 74–80, doi: 10.1177/228080000400200202.
[7] S. Hirai, S. Ishimoto, P. Phanthong, and S. Yao, “Development of surface properties of ultra-high-molecular-weight polyethylene film using side-chain crystalline block copolymers,” J. Polym. Eng., vol. 40, no. 3, pp. 231–236, Mar. 2020, doi: 10.1515/polyeng-2019-0311.
[8] S. M. Kurtz, “From Ethylene Gas to UHMWPE Component: The Process of Producing Orthopedic Implants,” in UHMWPE Biomaterials Handbook: Ultra High Molecular Weight Polyethylene in Total Joint Replacement and Medical Devices: Third Edition, 2015, pp. 7–20.
[9] Y. Chen, Y. Qi, Z. Tai, X. Yan, F. Zhu, and Q. Xue, “Preparation, mechanical properties and biocompatibility of graphene oxide/ultrahigh molecular weight polyethylene composites,” Eur. Polym. J., vol. 48, no. 6, pp. 1026–1033, 2012, doi: 10.1016/j.eurpolymj.2012.03.011.
[10] S. M. Kurtz and S. M. Kurtz, “UHMWPE biomaterials handbook : ultra high molecular weight polyethylene in total joint replacement and medical devices,” in UHMWPE Biomaterials Handbook, 2009.
[11] Z. Zheng, X. Huang, Y. Li, N. Yang, X. Wang, and M. Shi, “Influence factors of internal structure and interfacial compatibility of UHMWPE fiber/SEBS resin composites: Processing parameters, structure of fiber and nature of resin,” Compos. Part B Eng., vol. 43, no. 3, pp. 1538–1544, 2012, doi: 10.1016/j.compositesb.2011.11.011.
[12] S. Yousef, “Polymer Nanocomposite Artificial Joints,” in Carbon Nanotubes – Current Progress of their Polymer Composites, InTech, 2016.
[13] N. Mamidi et al., “Cytotoxicity evaluation of unfunctionalized multiwall carbon nanotubes-ultrahigh molecular weight polyethylene nanocomposites,” J. Biomed. Mater. Res. – Part A, 2017, doi: 10.1002/jbm.a.36168.
[14] A. Sobajima et al., “Multiwall Carbon Nanotube Composites as Artificial Joint Materials,” ACS Biomater. Sci. Eng., vol. 6, no. 12, pp. 7032–7040, Dec. 2020, doi: 10.1021/acsbiomaterials.0c00916.
[15] A. Yildrim and T. Seçkin, “In situ preparation of polyether amine functionalized MWCNT nanofiller as reinforcing agents,” Adv. Mater. Sci. Eng., vol. 2014, 2014, doi: 10.1155/2014/356920.
[16] P. G. Ren, S. Y. Hou, F. Ren, Z. P. Zhang, Z. F. Sun, and L. Xu, “The influence of compression molding techniques on thermal conductivity of UHMWPE/BN and UHMWPE/(BN + MWCNT) hybrid composites with segregated structure,” Compos. Part A Appl. Sci. Manuf., vol. 90, pp. 13–21, 2016, doi: 10.1016/j.compositesa.2016.06.019.
[17] P. S. R. Sreekanth and S. Kanagaraj, “Influence of multi walled carbon nanotubes reinforcement and gamma irradiation on the wear behaviour of UHMWPE,” Wear, vol. 334–335, pp. 82–90, 2015, doi: 10.1016/j.wear.2014.12.014.
[18] A. Sharifi et al., “Investigation of photocatalytic behavior of modified ZnS:Mn/MWCNTs nanocomposite for organic pollutants effective photodegradation,” J. Environ. Manage., vol. 247, pp. 624–632, Oct. 2019, doi: 10.1016/j.jenvman.2019.06.096.
[19] M. J. Martínez-Morlanes, P. Castell, V. Martínez-Nogués, M. T. Martinez, P. J. Alonso, and J. A. Puértolas, “Effects of gamma-irradiation on UHMWPE/MWNT nanocomposites,” Compos. Sci. Technol., vol. 71, no. 3, pp. 282–288, 2011, doi: 10.1016/j.compscitech.2010.11.013.
[20] A. Kropelnicki and W. J. Platt, “Failure of the Femoral Component in a Cemented Total Knee Replacement,” JBJS Case Connect., vol. 10, no. 4, p. e19.00362-e19.00362, 2020, doi: 10.2106/jbjs.cc.19.00362.
[21] A. E. Loeb, S. L. Mitchell, G. M. Osgood, and B. Shafiq, “Catastrophic Failure of a Carbon-Fiber-Reinforced Polyetheretherketone Tibial Intramedullary Nail: A Case Report,” JBJS case Connect., vol. 8, no. 4, p. e83, Oct. 2018, doi: 10.2106/JBJS.CC.18.00096.
[22] “Tomorrow’s technologies today – Nanovis.” https://nanovistechnology.com/ (accessed Jun. 09, 2021).
[23] “Наноапатит – Разработка и выпуск инновационных материалов.” https://nanoapatit.ru/ (accessed Jun. 09, 2021).
[24] “Start: Artoss.” https://www.artoss.com/ (accessed Jun. 09, 2021).
—————————————————
بخش ترویج صنعتی فناوری های نانو و میکرو
====================================================================================
(توجه: جهت دسترسی به گزارش نهایی محصولات و شرکتهای دارای گواهی نانومقیاس ستاد توسعه فناوریهای نانو و میکرو به «کتب مرجع محصولات و تجهیزات نانو و صنعت» به نشانی (INDnano.ir/category/book) مراجعه کنید)
همچنین برای دسترسی به فایل PDF کلیه گزارشات، به بخش گزارش های صنعتی پایگاه اینترنتی رسانه تخصصی نانو و صنعت (www.INDnano.ir/category/report) مراجعه نمایید.
====================================================================================
[18] Nano Boogy