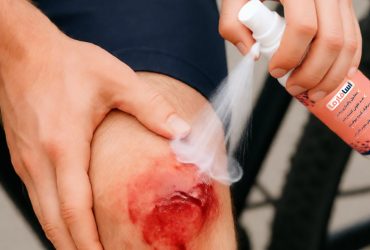
مدیریت و مراقبت از زخم عمدتاً به تولید مواد جدید و مؤثر در پانسمان زخم متکی است و همچنان تحقیقات گستردهای در زمینه مراقبت از زخمهای مزمن در حال انجام است. مدیریت مناسب مراقبت از زخم یک چالش کلینیکی قابل توجه است و نیاز فزایندهای به مراقبت از زخم وجود دارد. در سالهای اخیر، تحقیق و توسعه مواد پانسمان کننده زخم وارد سطح جدیدی از استانداردها شده است و درک بهتری از بیماریزایی[1] زخمهای مزمن وجود دارد. فناوری نانو با تحریک حرکت مناسب در مراحل مختلف بهبود، رویکرد فوقالعادهای برای تسریع در بهبود زخمهای حاد و مزمن ایجاد میکند. در فناوری نانو از مواد نانو کوچک، داربستهای نانو، الیاف نانو و مواد زیستی برای انتقال موضعی دارو برای بهبود زخمها استفاده میشود. در سالهای اخیر، استفاده از مواد نانو برای کاربردهای پزشکی و دارویی جذابیت قابل توجهی پیدا کرده است؛ بنابراین، درصد قابل توجهی از مواد نانو در کاربردهای مختلف زیست پزشکی برای پانسمان زخم، رهایش دارو و سایر اهداف پزشکی استفاده میشوند. این گزارش به بررسی کاربرد نانوذرات و نانومواد قابل تجزیه زیستی درترمیم زخمها خواهد پرداخت.
—————————
[1] pathogenesis
مقدمه
پوست بزرگترین و بیرونیترین عضوی است که کل بدن را پوشانده است (شکل 1)؛ بنابراین مهمترین وظیفه اصلی پوست محافظت از عضلات زیرین، استخوانها، رباطها و اندامهای داخلی در برابر عوامل زیستی، شیمیایی، مکانیکی و فیزیکی خارجی است [1]. علاوه بر این، پوست در ایجاد احساس، تنظیم دما، ایمنی، جلوگیری از اتلاف آب (کمبود آب) و سنتز ویتامین D3 نیز نقش دارد [2]. با این حال، ساختار و عملکردهای انجام شده توسط این اندام میتواند تحت تأثیر بریدگیها، سوختگیها، برشهای جراحی یا بیماریهایی مانند دیابت قرار گیرد؛ بنابراین بعد از به خطر افتادن ساختار پوست، باید ساختار و عملکردهای آن در اسرع وقت برای اطمینان از هموستاز[1] بدن دوباره احیا شود [3]. برای رسیدن به این هدف، فرآیند ترمیم زخم تقریباً بلافاصله پس از آسیب دیدگی پوستی آغاز میشود تا از خطر آلودگی باکتریایی جلوگیری شود. معمولاً پس از بروز این نوع آلودگی زخمهای غیر قابل بهبود اتفاق میافتند [3].
شکل 1- ساختار پوست انسان [4]
عفونتهای پوستی و بافت نرم (SSTI[2]) شایعترین انواع عفونتها هستند و تقریباً هر ساله در ایالات متحده 14 میلیون نفر را مبتلا میکنند [5]. بسته به علت و شدت حمله میکروبی، SSTIها میتوانند باعث عفونتهای جزئی سطحی و یا تهدیدکننده زندگی باشند [6].
در یک انسان سالم، با فعال شدن سیستم ایمنی بدن در برابر عوامل بیماریزا، از عفونت جلوگیری میشود. در این فرایند، ماکروفاژها مهاجرت به محل زخم را آغاز میکنند و متعاقباً فاگوسیتوز[3] پاتوژنها را انجام میدهند [7]. در مرحله بعدی، پاسخ ایمنی توسط فعال شدن لنفوسیتهای T کمک کننده[4] ترشح میشود که لیگانداینترفرون γ و CD40 ترشح میکند تا پاسخ سیستم ایمنی انطباقی و هومورال را برای کشتن و حذف باکتریهای مهاجم به صورت همزمان همراه کند [8].
با این حال، اگر سیستم ایمنی قادر به حذف پاتوژن نباشد، عفونت رخ داده و باعث خراب شدن بافت گرانوله[5]، فاکتورهای رشد و اجزای زمینه خارج سلولی (کلاژن، الاستین و فیبرین) میشود، بنابراین روند طبیعیترمیم زخم به خطر میافتد [9]. از این رو تولید پانسمانهایی که بتوانند از نفوذ باکتریها به داخل زخم جلوگیری کنند یا از رشد میکروارگانیسمها جلوگیری کنند، امری اساسی است. برای رسیدن به این هدف، روشهای مختلفی شامل مواد با فعالیت (ضدمیکروبی) آنتیباکتریالی ذاتی، سطوح اصلاح شده با ترکیبات ضدمیکروبی، برای تولید پانسمان زخم وجود دارد [10].
فناوری نانو یک زمینه نوظهور است که در بسیاری از برنامههای زیست پزشکی برای جلوگیری از بیماریهای مختلف استفاده میشود. فناوری نانو شاخهای از فناوری است که ماده را در مقیاس مولکولی یا سطح اتمی دستکاری میکند و آن دسته از موادی که اندازه مولکولی آنها از 1 تا 100 نانومتر است، به عنوان «نانو» تعریف میشوند [11]. خصوصیات مکانیکی، حرارتی و کاتالیزوری مواد نانو به راحتی و با افزایش یا کاهش نسبت سطح به حجم تغییر میکند و این ویژگیهای جدید امکان استفاده از مواد نانو را در بسیاری از زمینههای زیستی فراهم میکند. در نانوپزشکی از فناوری نانو در کاربردهای پزشکی استفاده میشود، مانند توسعه داروهای جدید و سیستمهای دارورسانی موثرتر، ایجاد حسگرهای زیستی نانوالکترونیکی و تصویربرداری درونتنی [12].
پیشبینی میشود بازار پانسمان زخم تا سال 2025 از 7 میلیارد دلار در سال 2020 به رقم 2/11 میلیارد دلار برسد. رشد این بازار عمدتاً ناشی از افزایش تصادفات جادهای، افزایش بروز زخمهای مزمن، جراحی و زخمهای ترومایی، میزان بالای سزارین در زنان مسن، افزایش بروز آسیبهای سوختگی و پیشرفتهای فناوری در پانسمان زخم است.
اطلاعات بازار زخمپوشها
در سال 2019، آمریکای شمالی بیشترین سهم از بازار زخمپوشها را به خود اختصاص داده است و انتظار میرود این روند تا سال 2025 ادامه یابد. افزایش جمعیت سالمندان، افزایش شیوع زخمهای مزمن، افزایش هزینههای مراقبتهای بهداشتی و حضور بازیگران اصلی بازار زخمپوش دراین ناحیه، باعث شده است سهم عمده آمریکای شمالی را در بازار جهانی زخمپوشها شاهد باشیم.
بازیگران برجسته بازار زخمپوشها، 3M (ایالاتمتحده)، Smith & Nephew plc (انگلستان)، Integra LifeSciences Holdings Corporation (ایالاتمتحده)، Mölnlycke Health Care AB (سوئد)، ConvaTec Group plc (انگلستان)، Coloplast A/S (دانمارک)، Hollister Incorporated (ایالاتمتحده) هستند.
3M (ایالاتمتحده) پیشرو در بازار جهانی پانسمان زخم است. این شرکت برای افزایش بیشتر سهم خود در بازار پانسمان زخم روی راهاندازی خط تولید و خرید محصول تمرکز دارد. 3M در مراقبت از زخمهای پیشرفته پیشگام است و بیش از 15 سال است که در بازار حضور دارد؛ این امر مزیت رقابتی آن را در بازار فراهم میکند. این شرکت روی افزایش مشتری و گسترش توانایی خود در بازارهای نوظهور و دست نخورده (مانند بهکارگیری فناوری نانو) تمرکز کرده است.
فرایند ترمیم طبیعی زخم
قبل از بررسی شرایط پاتولوژیک مختلف ترمیم، ابتدا باید روند ترمیم طبیعی زخم را بررسی کنیم. ترمیم زخم پاسخی اجباری به انواع محرکها است که روی پوست یا هر اندام دیگری تأثیر میگذارد. در مورد آسیب بافتی یا پوستی، یک سری آبشارهای[6] متوالی رخ میدهد که در نهایت منجر به ترمیم بافت طبیعی میشود [13], [14]. ترمیم زخم معمولاً به چهار مرحله مختلف یعنی مرحله هموستاز، التهاب، تکثیر و مرحله بازسازی تقسیم میشود (شکل 2) [15]. انواع مختلفی از سلولها، آنزیمها، سیتوکینها، پروتئینها و هورمونها در فرایندهای ترمیم بافت نقش دارند [16]. در محل آسیب، ترومبین باعث فعال شدن پلاکت میشود، به این وسیله پلاکتهای فعال شده فاکتورهای مختلف رشد را تولید میکنند و این عوامل رشد به نوبه خود باعث تکثیر و مهاجرت فیبروبلاست و مهاجرت سلولهای اندوتلیال عروقی به محل آسیبدیده میشوند [17].
شکل 2- مراحل ترمیم زخم (a) مرحله هموستاز (b) مرحله التهاب (c) مرحله تکثیر (d) مرحله بازسازی [4]
زخمهای مزمن
زخمهای مزمن فرایند ترمیم دچار اختلال را به نمایش میگذارند و باعث میشوند که زخمها ظرف 3 ماه بهبود نیابند. در این میان زخمهای بستر التیامناپذیر[7] (NHPU)، زخمهای وریدی[8] (VUs) و زخمهای پای دیابتی[9] (DFU) شایعترین موارد هستند [18]. VUs در اثر عملکرد نامناسب دریچههای خون یا انسداد رگها، عمدتاً در پاها ایجاد میشوند. در مقابل، NHPU آسیبهای پوستی و زمینهای در بافت است که در اثر فشار طولانیمدت پوست در افراد در بستر یا با تحرک محدود برای مدت زمان طولانی ایجاد میشود. DFU اغلب از چندین عارضه دیابت مانند تغییر شکل پا، بیماریهای شریانی محیطی و نوروپاتی[10] محیطی شروع میشود. نوروپاتی دیابتی نتیجه آسیب عصبی است که در اثر سطح کنترل نشده گلوکز خون ایجاد میشود و از حساسیت پوست میکاهد. تغییر شکل پا منجر به تشکیل کراتوز و پینه میشود و در نتیجه باعث تشدید زخم و حتی گانگرن[11] میشود. همچنین بیماران دیابتی تغییراتی در سیستم مویرگی (ضخیم شدن غشای پایه، کاهش اندازه مویرگ و…) دارند. با گذشت زمان، تغییرات در سطح گلوکز به انقباض عروقی و انعقادپذیری پلاسما، ایجاد بیماری شریانی انسداد، ایسکمی و تشکیل زخم (بیماری شریانی محیطی) کمک میکند. زخمهای غیر قابل بهبود تأثیر قابل توجهی برای بیماران و خانوادههای آنها دارند. این نوع زخمها باعث از دست دادن عملکرد، عوارض، درد شدید، عفونت، بستری شدن در بیمارستان و در بعضی موارد قطع عضو میشوند [19].
درمانهای فعلی زخمهای مزمن
درمان فعلی زخمهای مزمن به علت زخم بستگی دارد. در همه موارد، تمیز کردن کافی و زدودن زخم، کنترل عفونتهای احتمالی و استفاده از پانسمان زخم مورد نیاز است. درمانهای NHPU شامل پانسمانهایی است کهترمیم زخم را تسریع کرده و فشار بافت را تسکین میدهند. با این حال، DFUها و VU روی پانسمان که محیط مرطوب را برای بهبود زخم و فشردهسازی حفظ میکند، تمرکز میکنند [20].
روشهای درمانی جدید در درمان زخمهای مزمن
در دهه گذشته، پیشرفتهای چشمگیری در توسعه روشهای درمانی جدید مانند استفاده از افزودنیهایی مانند مولکولهای ضدمیکروبی، سیتوکینهای تنظیمکننده سیستمایمنی، microRNA (miRNA) یا اگزوزومها صورت گرفته است.
پانسمانهای پیشرفته که عامل ضدمیکروبی آزاد میکنند، مانند ید یا نقره، در کاهش بار باکتریایی در محل زخم مؤثر هستند. برخی از نمونههای تجاری موجود در اروپا و ایالاتمتحده Actisorb Silver220 و Iodosorb هستند. پپتیدهای
ضدمیکروبی قادر به کنترل التهاب و عفونت باکتریایی هستند و به عنوان پپتیدهای ترمیمکننده زخم عمل میکنند. این خصوصیات در فرمولاسیونهای موضعی جدید برای درمان زخمهای مزمن بسیار مطلوب هستند [21].
نیاز به سیستمهای رهش جدید در زخمهای مزمن: فناوری نانو
روشهای درمانی فعلی برای درمان زخمهای مزمن برای پوشش زخم، محافظت در برابر عفونت باکتریایی، از بین بردن بافت مرده، ایجاد رطوبت و جذب مایعات اضافه در موضع زخم است. پلتفورمهای فناوری نانو، به دلیل ویژگیهایی که دارند امیدواریها و مزایای جدیدی را در این زمینه نشان دادهاند. پیشرفتهای اخیر در فناوری نانو زمینههای جدیدی را در زمینه کاربردهای دارویی فراهم کرده است که امکان انتقال مولکولهای زیستی مانند DNA / RNA یا[12]GF را فراهم میکند که میتوانند در ترمیم مزمن زخم استفاده شوند. اندازه کوچک و خصوصیات فیزیکو شیمیایی آنها باعث رهش داخل سلولی این مولکولهای زیستی یا داروها میشود، از این عوامل در برابر تخریب محافظت میکند و نفوذ دارو را به داخل زخم افزایش میدهد. در واقع این سیستم نیمه عمر عوامل دارویی را افزایش و تعداد دفعات استفاده و هزینهها را کاهش میدهد. علاوه بر این، کپسوله کردن داروها و بیومولکولها در داخل نانوحاملها، پروفیلهای مختلف رهاسازی دارو را امکانپذیر میکند که میتواند با نیازهای ترمیم زخم مطابقت داشته باشد.
کاربردهای تجاری پانسمانها و زخمپوشهای نانویی
تولیدات بومی
باند پانسمان آنتیباکتریال (آجی کت):
این پانسمان توسط داروسازی عماد سهامیخاص (تأسیس 1381) به تولید انبوه رسیده است.
این باند پانسمان حاوی نانوذرات نقره با خاصیت آنتیباکتریال است. فرایند بهبود زخمها توسط عفونتهای باکتریایی به تأخیر میافتد؛ بنابراین پیشگیری و درمان عفونت بخش مهمی از بهبود زخم است. از باند پانسمان حاوی نانوذرات نقره، جهت پانسمان زخم با ایجاد خاصیت آنتیباکتریال استفاده میشود. این گاز به دلیل خاصیت آنتیباکتریالی قوی نانوذرات نقره به منظور کنترل عفونت در محل سوختگی و زخم کاربرد دارد و با آزادسازی آهسته یون نقره اثرات ضدمیکروبی و ضدالتهابی خود را اعمال میکند [22].
کاربردهای باند پانسمان آنتیباکتریال (آجی کت):
- سوختگیهای حاد؛
- زخمهای دیابتی حاد؛
- زخمهای بستر حاد؛
- زخمهای مزمن.
خصوصیات باند پانسمان آنتیباکتریال (آجی کت):
- حاوی نانوذرات نقره با اندازه زیر ۱۰۰ نانومتر
- فعالیت آنتیباکتریالی علیه دو باکتری Aureus و E. coli
کاربرد فناوری نانو در محصول
- نقره دارای خاصیت آنتیباکتریال مؤثری است و کاهش اندازه ذرات نقره باعث افزایش سطح تماس مؤثر در واکنش شیمیایی و افزایش سرعت پاسخدهی نقره به محیط میشود.
- میزان «فعالیت ضدباکتریایی» این محصول مطابق با استاندارد ملی «نساجی- تعیین فعالیت ضدباکتریایی در کالاهای نساجی» به شماره ISIRI 11070 مورد ارزیابی قرار گرفت که نتایج آن مطابق جدول 1 است:
جدول 1- میزان فعالیت ضدباکتریایی پانسمان آنتیباکتریال (آجی کت)
| فعالیت ضدباکتریایی | |
| حد قابل قبول استاندارد | 2 (معادل 99 درصد) |
| نمونه شاهد | 0 |
| نمونه نانو (اشرشیا کلی) | 71/1(معادل 1/97 درصد) |
| نمونه نانو (استافیلوکوکوس اورئوس) | 89/1 (معادل 9/98 درصد) |
فعالیت ضدباکتریایی، شاخصی از میزان توانایی محصول در از بین بردن باکتریهای در تماس با محصول است که از مقایسه لگاریتمی تعداد باکتریهای موجود روی نمونه شاهد و نمونه محصول بعد از 24 ساعت تماس با باکتری بهدست میآید. طبق استاندارد مذکور، هنگامیکه فعالیت ضدباکتریایی محصول بین 2 تا 3 باشد، اثرگذاری معنیدار است؛ اگر فعالیت ضدباکتریایی بیش از 3 باشد اثرگذاری قوی دارد.
توجه: از ابتدای سال 1396 استاندارد مذکور ملاک اثبات فعالیت ضدباکتریایی قرار گرفته است. تأیید این محصول در گذشته طبق ضوابط اجرایی آن زمان بوده ولی تمدید اعتبار آن مشروط به ارائه مستندات طبق این استاندارد خواهد بود.
ایمنی و بستهبندی
این پانسمان در ابعاد ۵×۵، ۵×۱۰، ۱۰×۱۰، ۱۰×۲۰، ۲۰×۲۰، ۳۰×۳۰، ۴۰×۴۰ و ۵۰×۵۰ سانتیمتر مربع بسته بندی میشود.
این پانسمان در پوشش پلیمری بستهبندی میشود.
این پانسمان در افرادی که به نقره یا نایلون حساسیت دارند نباید استفاده شود.
پد جاذب خون و آب حاوی نانودندریمر
این محصول توسط شرکت مسئولیت محدود طلیعه طب توحید تأسیس 1381 ساخته شده است.
شکل 3- پد پنبهای حاوی درختسان (دندریمر) PAMAM نسل صفر به منظور افزایش جذب خون
پانسمان به منظور تسهیل در بهبودی زخم، پیشیگیری از عفونت، جلوگیری از خونریزی و حفظ رطوبت زخم و حفاظت از ناحیه آسیبدیده در برابر صدمات مکانیکی مانند ضربه یا خراش، انجام میشود. در این فرایند مواد شوینده و ضدعفونیکننده به همراه چسب زخم، پنبه و گاز استریل و پد، مورد استفاده قرار میگیرد. پد لایههایی از پنبه، گاز و یا پارچهای دیگر است که قدرت جذب ترشحات را دارد و اغلب در معرض عوامل بیماریزا و میکروبی است. از این رو استفاده از یک وسیله جایگزین که مشکلات میکروبی و عفونی برای مصرفکنندگان ایجاد نکند، یکی از ضرورتهای حوزه پزشکی است. با اصلاح ساختار این پدها با استفاده از درختسانها (شکل 4) که نوعی مولکول نانومقیاس و دارای ساختار متقارن، همگن و کروی سهبعدی هستند، راندمان پدهای پزشکی در جذب خون، ایجاد خاصیت ضدمیکروبی، استحکام و جذب رطوبت افزایش پیدا میکند [23].
شکل 4- تصویر شماتیک دندریمر و نسلهای مختلف آن [24]
دندریمرها دـتهای از پلیمرهای پـر شاخه بوده که دارای تعداد زیادی گروه جانبـی هستند. پلیپـروپیلنایمین و پلـیآمیدوآمین دو دندریمر پرکاربرد هستند که دارای گروه انتهایی آمین هستند. این دندریمرها در محیط اسیدی پروتون جذب کرده و بدین ترتیب، خاصیت ضدمیکروبی از خود نشان میدهند. با استفاده از این مولکولها، خاصیت جذب پدهای پزشکی، متشکل از گازهای استریل، پنبهها و باندها افزایش یافته و خاصیت آنتیباکتریال به همراه دارند. پدهای پنبهای تولیدی شرکت طلیعه طب توحید با به کارگیری این مولکولها، بازده بالاتری در جذب خون فراهم کرده است.
خصوصیات پد جاذب خون و آب حاوی نانو دندریمر:
- حاوی درختسان نانومتری نسل یکم؛
- جذب خون در عملهای جراحی؛
- پوشاندن انواع زخمها به منظور جذب خون و محافظت در برابر عفونت.
کاربرد فناوری نانو در محصول
به منظور بررسی توزیع اندازه ذرات درختسان تولید شده، از روش تفرق پویای نور (Dynamic light scattering) استفاده شد. نتایج بیانگر وجود ذرات با ابعاد کمتر از 10 نانومتر به طور غالب و البته وجود تعداد اندکی از ذرات با ابعاد بیشتر از 100 نانومتر است. وجود این ذرات موجب افزایش کارایی پد در جذب خون شده است.
آزمون شبیهساز جذب خون با غوطهوری یک پد خام و یک پد حاوی دندریمر در محلول شبیهساز خون (شکل 5) در دمای 37 درجه سانتیگراد انجام شد. مطابق با شکل زیر رنگ تیرهتر پد حاوی دندریمر (شکل سمت چپ) بیانگر جذب بیشتر محلول شبیهساز خون است.
شکل 5- پد بدون دندریمر (سمت راست) و پد حاوی دندریمر (سمت چپ) بعد از غوطهوری در محلول شبیهساز خون
محصول مذکور نظر به بند 2-3 استاندارد ملی ایران شماره 12098 قابلیت قرارگیری در دسته درختواره – درختسان (Dendrimer) را دارد و همچنین بر اساس بند 2.2 استاندارد ISO/TS 27687 حاوی نانو شئ[13] است.
تولیدات سایر کشورها:
شرکتهای مختلفی در سراسر جهان اقدام به تولید انواع مختلفی از زخمپوشها با ابعاد و کاربریهای مختلف
کردهاند که در جدول 2 به برخی از آنها اشاره شده است. به طور مثال شرکت ASO group انواع مختلفی از
زخمپوشها را تولید کرده است که یک نمونه آن در جدول 2 اشاره شده است. از دیگر محصولات این شرکت میتوان به زخمپوشهای هیدروژلی اشاره کرد که در عین ایجاد خاصیت خنککنندگی محل زخم، تجمعات درون زخم را نیز جذب میکند و مانع از ایجاد عفونت میشود. نقطه مشترک تمام این محصولات استفاده از نانوذرات نقره است که به علت خواص ذاتی آنتیباکتریایی این نانوذره است. سعی شده است در این جدول محصولاتی از تمام کشورهای مختلف که در حال حاضر به صورت عمده در بازارهای جهانی موجود است، آورده شود.
جدول 2- برخی از تولیدات زخمپوشهای نانویی در جهان
| نام محصول | ماده نانویی | نام شرکت | کشور |
| ColActive® Plus | نقره (نانوذره/ نانوپودر) | Covalon Technologies Ltd | کانادا |
| ACTICOAT | نقره (نانوذره/ نانوپودر) | Smith & Nephew | انگلیس |
| AQUACEL® | نقره (نانوذره/ نانوپودر) | ConvaTec Inc | آمریکا |
| Puracol | نقره (نانوذره/ نانوپودر) | Medline Industries, Inc | آمریکا |
| CalciCare | نقره (نانوذره/ نانوپودر) | Hollister Incorporated | آمریکا |
| Hemoflex | نقره (نانوذره/ نانوپودر) | INMED | روسیه |
| Sheer with Antibacterial | نقره (نانوذره/ نانوپودر) | ASO Group | آمریکا |
| MANUKAtex | نقره (نانوذره/ نانوپودر) | ManukaMed | آمریکا |
| Antibacterial Dressings | نقره (نانوذره/ نانوپودر) | Hollister Wound Care | آمریکا |
| Cosmopor® | نقره (نانوذره/ نانوپودر) | HARTMANN GROUP | چین |
| Curad | نقره (نانوذره/ نانوپودر) | Medline Industries, Inc | آمریکا |
| CLO-SUR P.A.D | نقره (نانوذره/ نانوپودر) | CHS Interventional inc | کانادا |
| Hansaplast Aqua Protect | نقره (نانوذره/ نانوپودر) | Beiersdorf AG | آلمان |
انواع پانسمانهای مصنوعی موجود در بازارهای جهانی و مزایا و معایب آنها [25]:
هیدروکلوئید[14]:
نوع ماده: این نوع پانسمان دارای ساختار دو طرفه است؛ که لایه داخلی آن از ژلاتین، پکتین، کربوکسی متیل سلولز، الاستومرها و لایه بیرونی آن یک لایه ضدآب است.
کاربرد: زخم اگزوداتیو[15] کم یا متوسط: فشار، زخم دیابتی
مزایا: بدون درد برداشته میشود، رطوبت زخم را حفظ میکند، به قسمت خشک و مرطوب میچسبد.
معایب: برای زخمهای با تراوش بالا مناسب نیست. برای زخم عفونی و بافتهای نکروزی[16] بیفایده است.
نام شرکت/ برند: M, Tegaderm, comfeel3
هیدروژل[17]:
نوع ماده: متاکریلاتها،[18]PVP، ژلاتین، پکتین، کیتوزان
کاربرد: زخمهای مزمن خشک (رطوبت کم)، زخم با بافت نکروزی، زخم متوسط یا عمیق: زخمهای بستر و سایشی
مزایا: یک محیط مرطوب فراهم میکند، زخم را خنک میکند و درد را کاهش میدهد. برای زخمهای نکروزی و عفونی مفید است.
معایب: رطوبت کم، جذب کم
نام شرکت/ برند: Aquaclear, purilon gel, hypergel sterigel
آلجینات[19]:
نوع ماده: سدیم و نمکهای کلسیم آلجینات
کاربرد: زخم اگزوداتیو بالا و متوسط، زخم عمیق: دیابتی، بستر، سایشی، وریدی، سوختگی نوع II
مزایا: فراهم کردن محیط مرطوب، ویژگی آلرژیک کم، مفید برای زخمهای نکروزی و عفونی
معایب: رطوبت کم، کنترل دورهای برای زخمهای عمیق
نام شرکت/ برند: Algisite,Algoderm,Sorbsan
فوم[20]:
نوع ماده: فومهای سیلیکونی و پلییورتان
کاربرد: زخم اگزوداتیو بالا و متوسط، زخم عمیق: دیابتی، بستر، سایشی، وریدی، سوختگی نوع II
مزایا: گرما را عایق کرده و زخم را گرم میکند، باعث ایجاد فشار در زخم وریدی میشود.
معایب: ایجاد آلرژی در پوستهای نازک، برای زخم خشک و عفونی بیفایده است.
نام شرکت/ برند: Allevyn,Lyfoam,Tegafoam
فیلمهای نیمه تراوا[21]:
نوع ماده: پلییورتان شفاف و نیمهتراوا
کاربرد: به عنوان لایه دوم برای هیدروژلها و فومها، زخم بدون ترواش، زخم ناشی از جراحی
مزایا: لایه ضدآب، نفوذپذیر به اکسیژن، بخار و سدی در برابر عفونتها
معایب: برای زخمهای با تراوش زیاد، خونی، نکروزی و عفونی بیفایده است
نام شرکت/ برند: Tegaderm,hydrofilm,polyskin
خلاصه
پوست نقش مهمی در بدن دارد زیرا به عنوان سدی در برابر محیط خارجی عمل میکند و از اندامهای داخلی در برابر از دست دادن آب، عفونت و بیماری محافظت میکند. امروزه تقریباً همه به دلیل بریدگی، سوختگی، بیماریها (به عنوان مثال دیابت) یا مداخلات جراحی زخم پوستی را تجربه کردهاند. در برخی شرایط، این زخمها به راحتی توسط پاتوژنهای مختلف موجود در محیط اطراف، میتوانند آلوده شوند. زخمهای مزمن روند ترمیم مختل شدهای دارند و چندین ماه طول میکشد تا پیشرفت نشان دهند. این زخمها باعث درد، عفونت، هزینه و اغلب منجر به قطع عضو میشوند و همچنان به عنوان یک اپیدمی خاموش بیش از 40 میلیون نفر در سراسر جهان را تحت تأثیر قرار میدهند. صرف نظر از اینکه چه روش درمانی برای بهبود زخم انتخاب شده باشد، زخم باید با ماده مناسبی پوشانده شود که به طور کلی «پانسمان زخم» نامیده میشود. در این بررسی، پانسمانهای مختلف زخم و انواع آن به صورت خلاصه شده، معرفی شد. مهمترین عواملی که باید در طراحی پانسمان زخم مورد توجه قرار گیرد، سازگاری زیستی، عدم سمیت سلولی، مقاومت مکانیکی (در حالت مرطوب و خشک)، جذب آب، میزان تبخیر بخار آب، توانایی نفوذ گاز، مانع در برابر میکروارگانیسمها، ظرفیت جذب اگزودا، خواص ضدباکتریایی/ ضدمیکروبی ذاتی و چسبندگی مناسب به سطح زخم است. عملکرد پوششدهندههای زخم با ترکیب مواد مختلف از جمله پلیمرها و مواد معدنی میتواند افزایش قابل ملاحظهای یابد. به عنوان مثال، پلیمرهایی مانند پلییورتان محیط مناسبی را برای زخم فراهم میکنند، در حالی که مواد معدنی مانند نقره و ZnO ویژگیهای ضدباکتریایی در پانسمان ایجاد میکنند.
در سالهای اخیر انقلاب فناوری نانو بر تمام زمینههای زندگی بشر تأثیر گذاشته است. در زمینه پانسمان زخمها، مواد نانو ابعاد، نقش ویژهای در چندین زمینه مختلف دارند. خصوصیت مهم نسبت سطح به حجم زیاد مواد نانو، تعامل بسیار خوب با ترکیبات مهم در محیط زخم را امکانپذیر میکند. سلولهای میزبان به طور طبیعی با ECM تعامل دارند که توسط مواد در مقیاس نانو بهتر میتوانند تقلید شوند. پانسمانهای زخم باید دارای اندازه منافذ مناسب باشند تا امکان پخش مناسب آب و گازها فراهم شود. بخش مهم عملکرد پانسمانهای زخم جلوگیری از عفونت و تخریب سلولهای میکروبی است که موفق به نفوذ به زخم شدهاند. همچنین فعالیت ضدمیکروبی، ذاتی مواد نانو کاملاً شناخته شده است. انتقال سلولهای زنده به محل زخم راهی جدید برای مهندسی بافت و پزشکی ترمیمی است. بدون شک نانو پزشکی نقش مهمی در طراحی و ساخت پانسمانهای زخم حاوی سلولهای زنده خواهد داشت. با این حال، هزینه تولید و قیمت نهایی، یک عامل غیر قابل انکار در پانسمان زخمهای تجاری است. پیشرفت در تولید محصولات نانو در مقیاس بزرگ، تحت تأثیر طیف گستردهای از کاربردهای مدرن صنعتی، ادامه خواهد یافت و انتظار میرود که باعث تولید پانسمانهای اقتصادی و با کیفیت بالا شود.
———————————————–
منابع:
[1] D. Simões, S. P. Miguel, M. P. Ribeiro, P. Coutinho, A. G. Mendonça, and I. J. Correia, “Recent advances on antimicrobial wound dressing: A review,” European Journal of Pharmaceutics and Biopharmaceutics, vol. 127. Elsevier B.V., pp. 130–141, Jun. 01, 2018, doi: 10.1016/j.ejpb.2018.02.022.
[2] D. Sundaramurthi, U. M. Krishnan, and S. Sethuraman, “Electrospun nanofibers as scaffolds for skin tissue engineering,” Polymer Reviews, vol. 54, no. 2. Taylor and Francis Inc., pp. 348–376, Apr. 03, 2014, doi: 10.1080/15583724.2014.881374.
[3] A. Wen et al., “Skin tissue engineering advances in severe burns: review and therapeutic applications,” academic.oup.com, vol. 4, Dec. 2016, doi: 10.1186/s41038-016-0027-y.
[4] R. S. Ambekar and B. Kandasubramanian, “Advancements in nanofibers for wound dressing: A review,” European Polymer Journal, vol. 117. Elsevier Ltd, pp. 304–336, Aug. 01, 2019, doi: 10.1016/j.eurpolymj.2019.05.020.
[5] A. F. Cardona and S. E. Wilson, “Skin and Soft-Tissue Infections: A Critical Review and the Role of Telavancin in Their Treatment,” Clin. Infect. Dis., vol. 61, no. suppl_2, pp. S69–S78, Sep. 2015, doi: 10.1093/cid/civ528.
[6] “Paul: Advances in wound healing materials – محقق Google.” https://scholar.google.com/scholar_lookup?title=Advances in Wound Healing Materials%3A Science and Skin Engineering&author=W. Paul&publication_year=2015 (accessed Jun. 10, 2021).
[7] M. Mühlstädt, C. Thomé, and C. Kunte, “Rapid wound healing of scalp wounds devoid of periosteum with milling of the outer table and split-thickness skin grafting,” Br. J. Dermatol., vol. 167, no. 2, pp. 343–347, Aug. 2012, doi: 10.1111/j.1365-2133.2012.10999.x.
[8] F. Siedenbiedel and J. C. Tiller, “Antimicrobial polymers in solution and on surfaces: Overview and functional principles,” Polymers, vol. 4, no. 1. Molecular Diversity Preservation International, pp. 46–71, Jan. 09, 2012, doi: 10.3390/polym4010046.
[9] J. P. Burnham, J. P. Kirby, and M. H. Kollef, “Diagnosis and management of skin and soft tissue infections in the intensive care unit: a review,” Intensive Care Medicine, vol. 42, no. 12. Springer Verlag, pp. 1899–1911, Dec. 01, 2016, doi: 10.1007/s00134-016-4576-0.
[10] K. Vig et al., “Advances in skin regeneration using tissue engineering,” International Journal of Molecular Sciences, vol. 18, no. 4. MDPI AG, p. 789, Apr. 07, 2017, doi: 10.3390/ijms18040789.
[11] M. Ngiam, L. T. Nguyen, S. Liao, C. K. Chan, and S. Ramakrishna, “Biomimetic nanostructured materials – potential regulators for osteogenesis?,” Ann. Acad. Med. Singapore, vol. 40, no. 5, pp. 213–222, 2011.
[12] R. F. J.-N. Nanotechnology, B. and Medicine, and undefined 2005, “What is nanomedicine?,” Elsevier, Accessed: Jun. 06, 2021. [Online]. Available: https://www.sciencedirect.com/science/article/pii/S1549963404000048.
[13] I. Pastar et al., “Epithelialization in Wound Healing: A Comprehensive Review,” Adv. Wound Care, vol. 3, no. 7, pp. 445–464, Jul. 2014, doi: 10.1089/wound.2013.0473.
[14] A. Atala, D. J. Irvine, M. Moses, and S. Shaunak, “Wound healing versus regeneration: Role of the tissue environment in regenerative medicine,” MRS Bull., vol. 35, no. 8, pp. 597–606, Jan. 2010, doi: 10.1557/mrs2010.528.
[15] N. K. Rajendran, S. S. D. Kumar, N. N. Houreld, and H. Abrahamse, “A review on nanoparticle based treatment for wound healing,” Journal of Drug Delivery Science and Technology, vol. 44. Editions de Sante, pp. 421–430, Apr. 01, 2018, doi: 10.1016/j.jddst.2018.01.009.
[16] G. A. Duque and A. Descoteaux, “Macrophage cytokines: Involvement in immunity and infectious diseases,” Frontiers in Immunology, vol. 5, no. OCT. Frontiers Media S.A., p. 491, Oct. 07, 2014, doi: 10.3389/fimmu.2014.00491.
[17] N. Evans, R. Oreffo, E. Healy, … P. T.-J. of the mechanical, and undefined 2013, “Epithelial mechanobiology, skin wound healing, and the stem cell niche,” Elsevier, Accessed: Jun. 10, 2021. [Online]. Available: https://www.sciencedirect.com/science/article/pii/S1751616113001550.
[18] G. H. R. Ceilley, “Chronic Wound Healing: A Review of Current Management and Treatments,” Adv. Ther., vol. 34, doi: 10.1007/s12325-017-0478-y.
[19] C. K. Sen et al., “Human skin wounds: A major and snowballing threat to public health and the economy: PERSPECTIVE ARTICLE,” Wound Repair and Regeneration, vol. 17, no. 6. pp. 763–771, Nov. 2009, doi: 10.1111/j.1524-475X.2009.00543.x.
[20] L. E. Dickinson and S. Gerecht, “Engineered biopolymeric scaffolds for chronic wound healing,” Frontiers in Physiology, vol. 7, no. AUG. Frontiers Media S.A., Aug. 05, 2016, doi: 10.3389/fphys.2016.00341.
[21] M. L. Mangoni, A. M. Mcdermott, and M. Zasloff, “Antimicrobial peptides and wound healing: biological and therapeutic considerations,” Wiley Online Libr., vol. 25, no. 3, pp. 167–173, Mar. 2016, doi: 10.1111/exd.12929.
[22] “محصولات فناوری نانوایران – محصولات فناوری نانوایران | کالاها | پانسمان حاوی نانوذرات نقره با خاصیت آنتی باکتریال.” https://nanoproduct.ir/product/1811/باند پانسمان آنتی باکتریال (آجی کت) (accessed Jun. 07, 2021).
[23] “محصولات فناوری نانوایران – محصولات فناوری نانوایران | کالاها | پد پنبهای حاوی درختسان (دندریمر) PAMAM نسل صفر به منظور افزایش جذب خون.” https://nanoproduct.ir/product/2443/پد جاذب خون و آب حاوی نانو دندریمر (accessed Jun. 07, 2021).
[24] “Dendrimer – Wikipedia.” https://en.wikipedia.org/wiki/Dendrimer (accessed Jun. 07, 2021).
[25] P. Zarrintaj et al., “Can regenerative medicine and nanotechnology combine to heal wounds? the search for the ideal wound dressing,” Nanomedicine, vol. 12, no. 19. Future Medicine Ltd., pp. 2403–2422, Oct. 01, 2017, doi: 10.2217/nnm-2017-0173.
—————————————————————–
[1] هِموستاز (Hemostasis) یا خونایستی به قطع خونریزی به روشهای گوناگون گویند.
[2] Skin and soft tissue infections
[3] بیگانهخواری یا فاگوسیتوز (Phagocytosis) به بردن درشت مولکولها به داخل یاخته (سلول) و هضم آنها گفته میشود.
[4] lymphocytes T helper
[5] گرنولاسیون زخم به تشکیل بافت جدید و عروق خونی در محل زخم طی فرایند ترمیمیگفته میشود.
[6] cascade
[7] nonhealing pressure ulcers
[8] venous ulcers
[9] diabetic foot ulcers
[10] neuropathy
[11] gangrene
[12] Growth factor
[13] Nano-object
[14] Hydrocolloid
[15] زخم دارای ترواش را گویند.
[16] necrotic
[17] Hydrogel
[18] Polyvinylpyrrolidone
[19] Alginate
[20] Foam
[21] Semi-permeable film
—————————————————
بخش ترویج صنعتی فناوری های نانو و میکرو
====================================================================================
(توجه: جهت دسترسی به گزارش نهایی محصولات و شرکتهای دارای گواهی نانومقیاس ستاد توسعه فناوریهای نانو و میکرو به «کتب مرجع محصولات و تجهیزات نانو و صنعت» به نشانی (INDnano.ir/category/book) مراجعه کنید)
همچنین برای دسترسی به فایل PDF کلیه گزارشات، به بخش گزارش های صنعتی پایگاه اینترنتی رسانه تخصصی نانو و صنعت (www.INDnano.ir/category/report) مراجعه نمایید.
====================================================================================